Этиловый спирт – формула и применение. Формула спирта структурная
Формула спирта в химии
Определение и формула спирта
Спирты можно рассматривать как производные воды , в которых один атом водорода замещен на органическую функциональную группу.
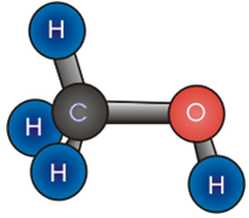
Общая формула спиртов:
Структурная формула метанола, простейшего спирта,
Соединения, в которых гидроксильная группа связана с ненасыщенным атомом углерода, по номенклатуре ИЮПАК (IUPAC) называются енолы (гидроксильная группа связана с двойной связью C=C). Соединения, в которых гидроксильная группа связана с бензольным или любым другим ароматическим циклом называются фенолы.
Классификация и структура спиртов
Формулы разных спиртов
Общая формула предельных одноатомных спиртов:
Общая формула двухатомных спиртов (гликолей, диолов):
Общая формула трехатомных спиртов (триолов):
Для многих спиртов наряду с систематическими часто употребляются тривиальные названия:

Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Урок в 10-м классе "Состав, строение, классификация, номенклатура и изомерия спиртов"
Разделы: Химия
Цели урока:
Обучающие:
- Изучение новых органических соединений, которые имеют в своём составе атомы химического элемента – кислорода и являются производными углеводородов;
- Изучить новое понятие “функциональная группа”;
- Рассмотреть состав, строение, гомологический ряд спиртов – алканолов;
- Познакомить учащихся с основами номенклатуры спиртов и типами изомерии у них; научить составлять структурные формулы спиртов;
- Познакомить учащихся с новым видом изомерии – изомерия положения функциональной группы.
Развивающие:
- Развивать интеллектуальные умения выделять главное, логически мыслить, делать выводы и обобщения;
- Продолжение формирования коммуникативных умений при работе в группах;
- Вовлечь каждого учащегося в процесс овладевания знаниями через организацию работы в группах.
Воспитательные:
- Продолжить формировать научное мировоззрение учащихся при изучении темы: “кислородсодержащие соединения”.
Ход урока
I. Вхождение в урок.
Учитель: Здравствуйте ребята. Я рада видеть вас сегодня на уроке. Сегодня мы начинаем изучать органические соединения, которые будут отличаться от ранее изученных органических веществ – углеводородов, составом и свойствами.
В состав многих органических соединений входят атомы кислорода. Первыми кислородсодержащими соединениями нами будут изучены спирты.
Но прежде чем мы начнем изучать спирты по известному плану: состав, строение, номенклатура, гомологический ряд, изомерия, физические и химические свойства, мне бы хотелось познакомить вас с интересными историческими сведениями.
Высвечиваются некоторые факты из исторической справки на мультимедийной установки (Приложение 1).
II. Исторические данные.
Учитель: Этанол (метилкарбинол, этиловый или винный спирт) известен человеку с глубокой древности. В те давние времена его называли и водой горючей, и водой жизни, и духом воина.
Ещё в IV веке до нашей эры люди умели приготавливать напитки, содержащие этиловый спирт. Вино получали сбраживанием фруктовых и ягодных соков.
В 11 веке алхимики обнаружили, что при нагревании вина, образуются пары летучего вещества, которые при охлаждении конденсируются в бесцветную жидкость со жгучим вкусом.
В 13 веке этанол стали использовать в медицине под названиями “мать”, “государыня”, “царица всех лекарств”.
В средние века этиловый спирт считался одним из сильнейших лекарственных, одно из первых его названий “жизненная сила”.
Потребление алкоголя в средние века было дурной привычкой, поэтому обычно употребляли пиво, и называли его “жидким хлебом”.
Впервые в XV веке слово алкоголь применялся к этанолу знаменитый немецкий врач, естествоиспытатель Теофраст Парацельс. Только в 1780 году (18 век) А.Лавуазье установил, что в состав этилового спирта входят углерод, водород, кислород, а молекулярную формулу С2Н6О определил в 1833 году Берцеллус.
III. Молекулярная и структурная формула спирта.
Учитель: Учёным понадобилось 53 года для выведения молекулярной формулы спирта, а я предлагаю вам, используя знания о продуктах сгорания этого вещества и математические формулы, вывести формулу одного из представителей класса спиртов за несколько минут.
Запишем условие в тетрадь:
Условие задачи записано на доске заранее, один учащийся решает её на доске (Приложение 2).
Учитель: В результате решения задачи нами определена молекулярная формула вещества С2 H6O . Молекулярная формула этого вещества не отражает принадлежности этого вещества к классу спиртов. Поэтому вам сейчас предлагается возможность предложить структурные формулы, соответствующие молекулярной формуле С2 H6O . Для этого вы объединитесь в группы по 4 человека, на столах у вас находятся листы, на которых вы предоставите свои результаты и мы сравним их.
Учитель отводит 5 минут для работы учащихся в группах, свои результаты ребята прикрепляют на доску, затем на экране высвечиваются возможные структурные формулы:
Учитель: Проанализируйте полученные формулы.
Ученик: В формуле (1) все атомы водорода равноценны, связаны - связями с атомом углерода; в формуле (2) один атом водорода соединен с атомом кислорода, то есть находится в особом положении; атомы водорода в этих веществах должны характеризоваться разными свойствами.
Учитель: Ребята, чтобы проверить этот вывод, посмотрим схему установки для демонстрации опыта “Выделение водорода из этилового спирта “ через мультимедийную установку.
Учитель включает мультимедийную установку со схемой реактора и комментирует рисунок:
Учитель: Рассмотрим рисунок. Главной частью прибора является реакционный сосуд, представляющий собой пробирку с раздвоением на два колена. В одно колено прибора налили 2,3 грамма этанола, что составляет 0,05 моль этого вещества. В другое колено положили кусочек натрия (небольшой избыток), приливают из одного колена в другое спирт. Наблюдается бурная реакция с выделением водорода. Выделяющийся газ вытесняет воду из двуглавого сосуда в мерный цилиндр. Экспериментально установлено, что:
Из 0,05 моль спирта – 0,56 л H 2, Из 1 моль спирта – Х литров h3. X = 11,2 литра h3 (1/2 моль)
Следовательно, из молекулы спирта выделится 1 атом водорода. Из этого сделаем вывод.
Учитель обращается к формулам (1) и (2), которые проецируются на экран.
Учитель: Рассмотрим ещё раз выведенные наши структурные формулы. Если этиловый спирт имеет формулу (1), то непонятно, почему из шести атомов водорода, входящих в состав метиловых групп, замещаются не шесть равноценных атомов водорода, а лишь один. В формуле (2) СН3 – СН2 – ОН один атом водорода занимает особое место, находясь в составе группы –ОН. Он не связан непосредственно с атомом углерода, как другие атомы водорода, а связан с атомом кислорода, который входит в состав функциональной группы –ОН и является более подвижным, легко замещается на атомы металла. Отсюда вывод: именно структурная формула0(2) СН3 - СН2 – ОН присуща этиловому спирту.
Учитель (обращаясь к классу): Теперь мы можем дать определение спиртов. Прочитаем это определение в слух из учебника на странице 130. Дома вы его выучите наизусть.
Учитель: Гидроксильная группа –ОН имеет определенное название – функциональная. Это определение находится на странице 42 учебника. Вспомним его.
Учащиеся зачитывают определение и записывают его в тетради.
IV. Изомерия, номенклатура спиртов.
Учитель: Ребята! Сегодня на уроке мы познакомимся с многообразием спиртов, в этом нам поможет их классификация. Она представлена в виде схемы и находится у вас на столах.
Учитель одновременно высвечивает её на экране с помощью мультимедийной установки.
Учитель: Эту схему вы вклеите себе в тетрадь, используя данную классификацию, охарактеризуйте следующие спирты:
С4Н9ОН – одноатомный, первичный, предельный (СН3-СН2-СН2-СН2-ОН)
Учитель: В таблице даны названия спиртов. Вы уже знакомы с номенклатурой углеводородов – алканов, алкенов, алкинов. Эти правила переносятся и на спирты, но здесь ещё учитывается положение гидроксильной группы в углеродной цепи. Согласно номенклатуре ИЮПАК название спиртов образуются добавлением суффикса –ол к названию соответствующего ему предельного углеводорода. Вспомним, как даются названия углеводородов.
Ученик: Сначала определим главную цепь, нумеруем атомы углерода в главной цепи с того конца, к которому ближе функциональная группа –ОН, затем определяем у каких атомов углерода находятся заместители и называем их, затем дадим название главной цепи, добавив в конце названия суффикс –ол и цифрой укажем у какого атома углерода находится гидроксильная группа.
Учитель: Ребята! У вас на столах находятся формулы спиртов, дадим им названия по систематической номенклатуре. (Приложение 3).
Трое учащихся отвечают на оценку, формулы спиртов написаны на доске.
Учитель: Начиная изучать органическую химию, мы с вами познакомились с теорией химического строения органических соединений А.М. Бутлерова. Одно из положений гласит, что свойства веществ зависят не только от их качественного и количественного состава, но и от того в каком порядке соединены атомы в молекуле, то есть от химического строения. Это положение знакомит нас с понятием изомерии. Вспомним, что такое изомерии, и какие вещества называются изомерами.
Ученик: Вещества, имеющие одинаковые состав, одинаковую молекулярную массу и формулу, но различное строение, а следовательно, и разные свойства, называются изомерами, а само явление – изомерии.
Учитель: Какие виды изомерии будут иметь спирты?
Ученик: Для них характерна изомерия углеродного скелета.
Учитель: В спиртах имеется функциональная группа –ОН, ее положение в молекуле спирта обуславливает новый вид изомерии – изомерия положения функциональной группы. Наличие таких изомеров у спиртов – это одна из причин их многообразия.
Ребята! Вам дана молекулярная формула С4Н9ОН. Составьте структурную формулу всех возможных изомеров спиртов, затем мы проверим полученные формулы на доске.
Отводится 3-4 минуты для составления формул, затем через мультимедийную установку проверяются формулы и их названия (Приложение 4).
Учитель: Ребята, на доске оставлены структурные формулы, которые мы с вами вывели, исходя из математических расчетов. Они позволяют определить третий вид изомерии спиртов – межклассовая изомерии, предельные одноатомные спирты изомерны простым эфирам.
Рассмотрим возможные формулы эфиров, соответствующие молекулярной формуле С4Н10О.
СН3 – О – С3Н7 —> метилпропиловый эфир; С2Н5 – О – С2Н5 —> диэтиловый эфир.
Знания изомерии спиртов вы закрепите в процессе выполнения домашней работы.
V. Заключительная часть.
Учитель: Ребята! Наш урок подходит к завершению. В начале урока перед вами были поставлены задачи: ознакомиться с новым классом органических соединений – спиртами, наличием в их строении функциональной группы –ОН, рассмотреть состав, строение, виды изомерии и номенклатуры спиртов. Настало время подвести итоги. Что нового сегодня узнали на уроке? Чему научились?
Ученик: На уроке мы познакомились с новы классом органических, кислородсодержащих соединений – спиртами. Выяснили их строение, наличие функциональной группы –ОН, появление нового вида изомерии – изомерия положения функциональной группы; познакомились с классификацией спиртов.
Учитель: Ребята, а теперь я хочу предложить вам небольшую самостоятельную работу, с помощью которой мы закрепим знания, полученные по составлению формул изомеров спиртов и их номенклатуре.
Задания записаны на доске (Приложение 5). На работу отводится 5-7 минут.
Учитель: Ребята, знания, полученные сегодня на уроке пригодятся нам на следующих уроках при изучении других классов органических соединений. Осталось записать домашнее задание: параграф 21, вопросы на странице 135 с 1 по 3 устно, упражнения 6 – 8 письменно.
Список литературы:
- Кузнецова Н.Е., Титова И.М., Тара Н.Н. Химия: Учебник для учащихся 10 класса общеобразовательных учреждений (под редакцией Кузнецовой Н.Е.). – М.: Вентана-Граф, 2004. – 384 с.:ил
- Артемьев А.И. Удивительный мир органической химии. – М.: Дрофа, 2004. – 256 с.: ил – (Познавательно! Занимательно!)
- Габриелян О.С., Маскаев Ф.Н.Химия 10 класс: Учебник для общеобразовательных учреждений. 3-е издание стереотип. – М.: Дрофа, 2002
- Кириллова Е.Н., Иозеп А.А. Домашние задания по органической химии. Под ред. проф. Д.А.Ивина.- С-Пб.: из-во СПХФА, 2003
- Аранская О.С., Бурая И.В. Проектная деятельность школьников в процессе обучения химии 8 – 11 классы.: Методическое пособие. – М.: Вентана-Граф, 2005
- Титова И.М. Обучение химии. Психолого-методическое пособие. – С-Пб.: Каро, 2002
- Артёминко А.И. Удивительный мир органической химии. – М.: Дрофа, 2004
- Органическая химия: Теоретические основы: Углубленный курс. Учебник для общеобразовательных учреждений с углубленным изучением предмета. – М.: Просвещение, 1997
- Пичугина Г.В. Химия и повседневная жизнь человека. – М.: Дрофа, 2004
- Малышкна В. Занимательная химия. – С-Пб.: Тригон, 2001
xn--i1abbnckbmcl9fb.xn--p1ai
Формула этилового спирта, химический состав этанола
Рассмотрим формулу такого вещества, как спирт этиловый, кто и когда ее вывел. Американский художник Марк Келлер заметил, что у спирта много лиц. Ведь это и продукт питания, и жидкое топливо, и медицина. Те, кто увлекается наукой об элементах, уже догадались, что речь идёт о самом древнем веществе – этаноле. Считается, что появился этанол или этиловый спирт около четырёх тысяч лет назад в давних государствах с высоким уровнем цивилизации – Древний Египет и Вавилон. У него очень много родственников и большая популярность в мире.
Экскурс в прошлое этанола

Предлагаем окунуться в мир химии и узнать больше об одном из известнейших элементов. Вдруг окажется, что вы знаете не так много о нём?
Первым спиртом, который человек открыл и начал использовать, был этанол. К сожалению, история не сохранила для потомков имени этого человека. Легенды говорят о том, что впервые вещество было получено из виноградного сока, а случилось открытие в XI столетии. Позже изобретатели алкоголя были удивлены его чудесными свойствами. Такие качества нового открытия подтолкнули их к мысли назвать вещество «благородный».
С давних времён этанол можно было найти в напитках, лекарствах. В проведении некоторых религиозных обрядов его тоже использовали. В стране пирамид перерабатывали растительные продукты, добывая это вещество. Но так получался только его раствор. Чтобы увеличить его насыщенность, древние китайцы начали перегонять вещество. Открыли этот процесс более девяти тысяч лет тому назад. Около десяти тысяч лет назад открытием этанола на территории стран Востока послужил виноград. Подтверждение этому – надписи на табличках-кирпичиках Междуречья.
В Средние века алкоголь был главной основой в приготовлении различных лекарств. На латыни средневековые учёные-химики называли его «живая вода».
Только в конце XVIII века русскому учёному-химику Ловицу удалось провести химический эксперимент, получив чистый этанол. В начале XIX столетия швейцарский учёный получил химическую формулу этилового спирта, а через пятьдесят лет профессор из Швейцарии предложил его химическое строение и это, безусловно, был большой прорыв в науке.
к содержанию ↑Формула вещества или немного науки
Химическое название этого вещества – этиловый спирт, а латинское название – этанол.
Общая химическая формула вещества – С2H5OН.
О чём говорит для непосвященных в этой науке химическая формула?
Его химический состав – три молекулы:
С – углерод и два его атома.
Н – водород и пять атомов.
ОН – гидроксильная группа.
Позже была предложена структурная формула этилового вещества: Ch4CН2OH. Эта химическая формула говорит о том, что этанол – насыщенное вещество.
За физическими качествами этиловый спирт – жидкость без цвета, легко испаряется, имеет характерный запах, палящий вкус.
Химические качества его таковы:
- легко загорается, выделяя при этом тепло; при большом количестве воздуха пламя окрашивается в голубоватый цвет;
- вступает в реакцию отщепления молекул воды с серной кислотой;
- реагирует с классом карбоновых кислот, образуя сложные эфиры;
- взаимодействует со щелочными металлами.
Как же получают этанол?
Перечислим основные способы:
- брожение продуктов органики, например, винограда. Под действием бактерий получается около 15% этанола;
- производство в современной промышленности даёт возможность добыть более 95% этанола. Для такого синтеза используют растения, состав которых крахмал, пшеница, картофель, кукуруза;
- также вещество получают из древесины, целлюлозы, используя химическую реакцию их взаимодействия с водой.
Где используют этанол?
Наверное, трудно назвать какую-либо отрасль, где бы ни упоминался химический состав С2H5OН, ведь это вещество имеет огромный спектр применения. В медицине он просто незаменим, выполняя роль и консерванта, и растворителя. Для уничтожения инфекций это вещество – уникальное средство во время проведения хирургических операций. Некоторые настойки, например, валерьянка, сохраняются длительное время именно благодаря С2H5OН.
Ракетные двигатели не могут эффективно работать без этилового спирта. Ведь топливом для них служит С2H5OН.
В промышленности он – химический состав для растворителей, лаков, в некоторых бытовых средствах для чистки сантехники в составе тоже присутствует С2H5OН.
Как известно, одна из проблем современного человечества – автомобильные выхлопные газы. Так вот в Бразилии эту проблему учёные-химики разрешили таким образом: к автомобильному горючему добавляют этанол. В этой стране почти половина всех автомобилей работает на чистом этаноле, который получают с помощью микроорганизмов из сахарного тростника.
Не обходится и косметика без этилового спирта. В таких косметических средствах, как одеколон, духи, дезодоранты, на этикетках найдётся в химическом составе этиловый спирт.
Этанол – это и различный алкоголь. Но в некоторые напитки, для изготовления которых используют брожение, в состав тоже входит алкоголь. Речь идёт о квасе, кефире, безалкогольном пиве. Содержание алкоголя в них меньше 0,2 %. Находясь долгое время в тёплом месте, состав алкоголя в них возрастает даже до 2%.
Конечно, теперь все знают, что в состав почти всех кондитерских изделий входят консерванты. Эту роль исполняет С2H5OН.
к содержанию ↑Этанол для человека: вред или польза?
Спирт, попадая в организм человека через органы пищеварения, быстро всасывается. Через пять минут он распространяется, действуя негативно на все органы человека.
- Точный удар по нервам:
В больших количествах может подавлять действие нервной системы.
Хроническое употребление этанола вызывает нехватку так называемого гормона счастья – серотонина.
Действие этилового элемента понижает остроту зрения и слуха, изменяет координацию движений человека, угнетает эмоциональное состояние.
- Уничтожение лёгких:
Ярко выраженное токсическое действие. Защитные функции организма уменьшаются, поэтому поражаются лёгкие и развивается лёгочная инфекция.
Возникает патология бронхов, которая может перерасти в воспаление лёгких. Отмечается при этом большая часть смертельных исходов после этих осложнений.
- Простой способ избавления от желудка:
Уже через некоторое время после попадания в организм вызывает воспаление слизистой оболочки желудка, похожее происходит и с двенадцатиперстной кишкой. Степень поражения печени напрямую зависит от количества выпитого алкоголя. Его последствия – патологическая жировая дистрофия печени, развитие алкогольного цирроза печени. Международные исследования подтвердили, что алкоголь влечёт за собой образование злокачественных опухолей.
- Прямое попадание в сердце:
Особенно чувствительны к влиянию веществам этанола люди с сердечно-сосудистыми болезнями. Такие люди, выпив даже небольшое количество алкоголя, могут умереть. После длительного употребления появляются патологические изменения сердца. Стенки сосудов утолщаются, нарушается питание сердечной мышцы. Многие алкоголики умирают от обширных инфарктов через отмирание сердечной мышцы.
Послушаем мнение экспертов.
Во всём мире давно существует химический способ производства этанола. Это ценное вещество используют во многих сферах жизни. Публикуются тысячи научных работ, в которых речь идёт о пользе и вреде С2H5OН. С одной стороны, небольшие дозы этанола приносят пользу организму человека: улучшают кровоснабжение, расширяют сосуды. Но только небольшое количество. С другой стороны, можно ещё раз вспомнить о том, что от пьющих родителей рождаются умственно отсталые дети, что тот же спирт – медленная смерть для человека.
Кто-то заметил, что после того, как химик Д. Менделеев разбавил С2H5OН с водой в определённых пропорциях, многое изменилось. Английский профессор Г.Эдвардс заметил, что алкоголь везде одинаков.
Неважно, какой алкоголь вам нравится: дорогой или дешёвый. Негативный исход зависит от того, какое количество его вы употребили и насколько часто пьёте.
Американские учёные исследовали, что автомобили на этаноле выбрасывают в воздух озон. Это основной ингредиент смога. Чем больше смога в воздухе, тем больше его негативное влияние на здоровье человека.
Эксперт А. Флеминг этиловый спирт остроумно называет «прекрасный яд». Бесспорно, мнения об этаноле разные. Польза или вред любого вещества зависит, для чего и с какой целью оно применяется. Но эксперты подводят к выводу: чем меньше употребляется алкоголя, тем лучше для государства и самого человека.
alcogolizm.com
Формула Бутилового спирта структурная химическая
Структурная формула
Истинная, эмпирическая, или брутто-формула: C4h20O
Рациональная формула: Ch4(Ch3)3OH
| C | Углерод | 12,011 | 4 | 64,8% |
| H | Водород | 1,008 | 10 | 13,6% |
| O | Кислород | 15,999 | 1 | 21,6% |
Молекулярная масса: 74,122
Бутанол-1(н-бутанол, н-бутиловый спирт) C4H9OH — представитель одноатомных спиртов. Известны нормальный первичный бутиловый спирт Ch4(Ch3)3OH и его изомеры: нормальный вторичный бутиловый спирт Ch4Ch3СН(ОН)СН3OH, изобутиловый спирт (Ch4)2СНСН2ОН, третбутиловый спирт (триметилкарбинол) (СН3)3СОН.
Физические свойства
Бесцветная вязковатая жидкость с характерным запахом сивушного масла. Смешивается с органическими растворителями. В отличие от метанола, этанола и пропанола только умеренно растворяется в воде — 7,6 г на 100 г воды. С ней образует азеотроп содержащий 42,5 % по массе бутанола и кипящий при 97,7 °C.
Производство
В промышленности бутанол получают:
- оксосинтезом из пропилена с использованием никель-кобальтовых катализаторов при 1,0-1,5 МПа(По Реппе).
- Из ацетальдегида через ацетальдоль и кротоновый альдегид, который гидрируют на медных, меднохромовых или никелевых катализаторах.
- Ацетоно-бутиловым брожением пищевого сырья.
Историческая справка
Бутанол начал производиться в 10-х годах XX века с использованием бактерии Clostridium acetobutylicum. Сырьём для производства могут быть сахарный тростник, свекла, кукуруза, пшеница, маниока, а в будущем и целлюлоза. В 50-х годах из-за падения цен на нефть начал производиться из нефтепродуктов. В США ежегодно производится около 1,39 млрд литров бутанола.
Очистка и сушка
Существует несколько способов очистки бутанола в лаборатории:
- обычная фракционная перегонка с отделением азеотропа
- сначала кипятят 4 часа над свежепрокалённой жженой известью без доступа влаги (30 г на 1л), затем кипятят над магниевой стружкой. После спирт перегоняют и собирают фракцию 117,70±0,01 °C
- промыванием раствором бисульфита натрия, затем кипячением над 10 % водной натриевой щелочью и наконец тройным трёхчасовым кипячением над жженой известью с последующей фракционной перегонкой
Применение
Бутанол применяют:
- как растворитель в лакокрасочной промышленности, в производстве смол и пластификаторов
- модификаторы мочевино- и меламино-формальдегидных смол
- для получения пластификаторов: дибутилфталата, трибутилфосфата
- для получения бутилацетата и бутилакрилата и эфиров с гликолями
- в синтезе многих органических соединений.
Применение в качестве автомобильного топлива
Может, но не обязательно должен, смешиваться с традиционными топливами. Энергия бутанола близка к энергии бензина. Бутанол может использоваться в топливных элементах, как сырьё для производства водорода. В 2007 году в Великобритании начались продажи биобутанола в качестве добавки к бензину.
Безопасность
Токсичность бутанола относительно невелика (LD50 составляет 2290-4360 мг/кг), но наивысшая среди младших спиртов. При употреблении внутрь возникает эффект, сходный с эффектом от употребления этанола. Бутанол содержится в небольших количествах в различных алкогольных напитках. Иногда бутанол, полученный из технических жидкостей, используется в качестве суррогатного алкогольного напитка. Концентрация в 0,01 % в воздухе никак не влияет на организм, в то время как 0,02 % вызывает воспаление роговой оболочки глаза. КПВ 1,7-12 %.
formula-info.ru
Формула этилового спирта в химии
Определение и формула этилового спирта

Формула –
Молярная масса равна г/моль.
Физические свойства – бесцветная летучая горючая жидкость с характерным спиртовым запахом, имеющая жгучий вкус.
Смешивается с водой в любых соотношениях и образует с ней нераздельно кипящую смесь, которая имеет состав 95,57% спирта и 4,43% воды.
В технике этанол занимает первое место по объему производства среди других органических веществ.
Химические свойства этилового спирта
- Для этанола характерны слабые кислотные свойства, которые проявляются при взаимодействии с щелочными металлами. При этом образуются алкоголяты и происходит выделение газообразного водорода:
- Этанол легко воспламеняется и горит при достаточном поступлении воздуха голубоватым пламенем:
- Вступает в катализируемую сильными минеральными кислотами обратимую реакцию этерификации с карбоновыми кислотами с образованием сложного эфира и воды:
- Этиловый спирт реагирует с галогеноводородами:
- Этанол по-разному обратимо ведет себя при нагревании с водоотнимающими средствами:
Качественной реакцией на этанол является йодоформная проба. При взаимодействии спирта, йода и щелочи происходит образование желтоватого осадка йодоформа:
Способ получения этанола основывается на брожении сахаристых веществ (виноградного сахара) под влиянием энзимов и дрожжей. Общую схему можно представить как:
Данный способ является весьма неэкономичным, поэтому стоит задача полной замены пищевых продуктов непищевым сырьем. Здесь существует два основных направления. Первый, замена крахмала (целлюлозы) клетчаткой. Второй — синтез спирта из этилена его гидратацией.
Применение
Этиловый спирт в огромных количествах используется в производстве дивинила, этилового эфира, хлороформа, этилацетата и других сложных эфиров, используемых в качестве растворителей лаков и душистых веществ.
Также этанол применяется в качестве растворителя в производстве фармацевтических, душистых, красящих веществ. Этанол — очень хорошее антисептическое средство.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Структурная формула - спирт - Большая Энциклопедия Нефти и Газа, статья, страница 1
Структурная формула - спирт
Cтраница 1
Структурная формула спирта позволяет предсказать ход реакций с другими веществами, например, с галогеноводородными кислотами. [1]
Какова структурная формула спирта, в который фруктоза переходит при юсстановлении. [2]
Какова структурная формула спирта, в который фруктоза превращается при восстановлении. [3]
Какова структурная формула спирта, в который фруктоза переходит при восстановлении. [4]
Напишите структурные формулы спиртов: а) 2 3-диметил - З - гексанола, б) 2 3 4-триметил - З - пентано-ла, в) 2 4 4-триметил - 2-пентанола, г) 2 2 4 4-тетраметил - 3-пентанола, д) 2 5-диметил - 3-гексен - 2 5-диола. [5]
Каковы структурные формулы следующих спиртов: 1) изоамилового спирта, 2) аллилового спирта, 3) грег-бутилового спирта, 4) изопропилового спирта, 5) 2-метилгексанола - З, 6) 2 3-диметилбутанола - 2, 7) бу-тандиола-1 3, 8) гексантриола-1 3 4, 9) глицерина, 10) этиленгликоля. [6]
Напишите структурные формулы следующих спиртов: - диэтилфенилкарбинола, этил-о-толилкарбинола, изопропилфенил - - карбинола, диметилбензилкарбинола. [7]
Приведите простейшие структурные формулы спирта, альдегида и кислоты, полученных из метана; этана; бутана; октана. [8]
Напишите структурные формулы изомерных пенти-ловых спиртов СбНцОН и назовите их как производные метанола и по современной заместительной номенклатуре. Укажите, какие из этих спиртов являются первичными, вторичными, третичными. [9]
Написав структурную формулу синтезируемого спирта, можно легко выбрать соответствующие компоненты реакции н таким образом решить задачу получения спирта магнийорганнче-4 скнм синтезом. [10]
Написав структурную формулу синтезируемого спирта, можно легко выбрать соответствующие компоненты реакции и таким образом решить задачу получения спирта магнийорганиче-ским синтезом. [11]
Написав структурную формулу синтезируемого спирта, можно легко выбрать соответствующие компоненты реакции и таким образом решить задачу получения спирта ма нийорганиче-ским синтезом. [12]
Написав структурную формулу синтезируемого спирта, можно легко выбрать соответствующие компоненты реакции и таким образом решить задачу получения спирта магнийорга-ническим синтезом. [13]
Для подтверждения структурной формулы спирта важно установить, что образование молекулы воды происходит за счет одной, а не двух молекул спирта. [15]
Страницы: 1 2
www.ngpedia.ru
Этиловый спирт: формула, состав и варианты использования
Главная страница » Алкогольные напитки Просмотров: 285 Этиловый спирт является одним из наиболее древних веществ, появившийся около 4 тысяч лет назад в Вавилоне и Древнем Египте. Художник Марк Келлер говорил о том, что этанол многолик, поскольку его употребляют в пищу, используют в медицине и в качестве жидкого топлива. И это действительно так. Поэтому стоит подробнее остановиться на химической структуре этого вещества и рассмотреть его влияние на человеческий организм.
Этиловый спирт является одним из наиболее древних веществ, появившийся около 4 тысяч лет назад в Вавилоне и Древнем Египте. Художник Марк Келлер говорил о том, что этанол многолик, поскольку его употребляют в пищу, используют в медицине и в качестве жидкого топлива. И это действительно так. Поэтому стоит подробнее остановиться на химической структуре этого вещества и рассмотреть его влияние на человеческий организм.
Исторические факты
Этанол был первым видом спирта, который открыли люди и начали использовать в быту. По легенде, впервые этиловый спирт был получен из сока винограда в 11 веке. Уже позднее начали вскрываться удивительные свойства этого вещества, что подтолкнуло изобретателей называть его «благородным веществом». Действительно, этанол издавна использовался в лекарственных средствах и всевозможных напитках, его применяли в религиозных обрядах.
В Древнем Египте спирт добывали путем переработки различной растительной пищи, однако таким образом можно было выделить только раствор этанола. Для усиления концентрации в Китае было придумано подвергать раствор этилового спирта перегонке, которую изобрели около 9 тысяч лет назад.
Долгое время этиловый спирт был частью всевозможных лекарств, поэтому латинским названием этанола было слово, означающее в переводе «живую воду». И только в 18 веке русскому химику Ловицу удалось выделить чистый этиловый спирт из раствора.Уже в 19 веке один швейцарский ученый смог получить химическую формулу вещества, а другой, спустя 50 лет, вывел химическое строение этанола.
Химический состав
Этиловый спирт – это химическое название полученного вещества, а этанол – его латинское обозначение. В формуле этилового спирта имеются три молекулы – 2 атома углерода, 5 атомов водорода и гидроксильная группа ОН. Химическая формула этилового спирта выглядит следующим образом – С2Н5ОН, а его структурная формула – СН3СН2ОН, что говорит о насыщенности этанола. К физическим качествам этилового спирта относится бесцветность, жидкая структура, легкая испаряемость, характерный запах и обжигающий вкус.
К основным химическим качествам вещества можно отнести следующие:
- легковоспламеняемость с выделением теплоты;
- окрашивание пламени при возгорании на открытом воздухе в голубой цвет;
- вступает в реакцию с серной кислотой, отщепляя молекулы воды;
- вместе с классом карбоновых кислот образует сложные эфиры;
- вступает во взаимодействие с щелочными металлами.
 К основным способам получения этилового спирта в химии относят:
К основным способам получения этилового спирта в химии относят:
- процесс брожения органических продуктов, в результате которого возможно получить до 15% чистого этанола;
- промышленное производство с использованием растительного сырья на сегодняшний день дает около 95% этилового спирта;
- химическую реакцию, в которую вступает целлюлоза (древесина) и вода.
Область использования вещества
Молекулярная формула этилового спирта широко применяется в медицине, топливно-энергетическом комплексе, промышленности, косметологии и пищевой отрасли. Этиловый спирт – отличный уничтожитель многих бактерий и инфекций, он способен выполнять функцию консерванта и растворителя. Топливо для ракетных двигателей производится на базе формулы этилового спирта. В промышленности этанол применяется повсеместно, его вводят в состав большинства растворителей, лаков, красок, средств бытовой химии. В Бразилии для решения проблемы выхлопа газов в автомобильное топливо стали добавлять этанол, получаемый из сахарного тростника. Химическая формула этилового спирта присутствует во многих видах косметики, например, духах, одеколонах, лосьонах и тониках. Ну а в пищевой промышленности главное место для этанола отведено алкогольным изделиям, однако, в качестве консерванта его применяют и для производства большинства кондитерских изделий.
Для быстрого и надежного избавления от алкоголизма наши читатели советуют Препарат "Алкобарьер" . Это натуральное средство, которое блокирует тягу к спиртному, вызывая стойкое отвращение к алкоголю. Кроме того, Алкобарьер запускает восстановительные процессы в органах, которые начал разрушать спирт. Средство не имеет противопоказаний, эффективность и безопасность препарата доказана клиническими исследованиями в НИИ Наркологии. Узнать больше... »Воздействие на человеческий организм
Этиловый спирт, попадая в человеческий организм, начинает активно всасываться и распространяться по всем системам, негативно воздействуя на здоровье. Токсическое свойство спирта может проявляться в виде тошноты, головокружений, потери памяти, сердцебиения, рвоты, похмельного синдрома.
 При частых употреблениях алкоголя нарушаются обменные процессы в организме, страдает функция печени и почек, сердечно-сосудистая система. Однако, наиболее остро страдает центральная нервная система, поскольку регулярное употребление алкогольных напитков подавляет ее и приводит к угнетенным функциям слуха, зрения, ухудшению настроения, длительным депрессиям, нарушению координации движений. При длительном алкоголизме этанол способен полностью остановить выработку серотонина, который отвечает за эмоциональное состояние человека.
При частых употреблениях алкоголя нарушаются обменные процессы в организме, страдает функция печени и почек, сердечно-сосудистая система. Однако, наиболее остро страдает центральная нервная система, поскольку регулярное употребление алкогольных напитков подавляет ее и приводит к угнетенным функциям слуха, зрения, ухудшению настроения, длительным депрессиям, нарушению координации движений. При длительном алкоголизме этанол способен полностью остановить выработку серотонина, который отвечает за эмоциональное состояние человека.
Химическая формула этанола способна оказать выраженное токсическое воздействие на легкие человека. При употреблении спиртного угасают защитные функции организма, в результате чего происходит поражение легких и возникает легочная инфекция. Данная инфекция может привести к пневмонии, которая нередко заканчивается летальным исходом.
Первым под удар этилового спирта и его токсического воздействия всегда попадает желудочно-кишечный тракт, где поражается слизистая желудка и двенадцатиперстной кишки. Печень страдает при частом и обильном употреблении алкоголя, развивается цирроз, который также может закончиться смертельным исходом. К тому же, согласно многочисленным медицинским исследованиям, злоупотребление алкогольными напитками приводит к возникновению онкологических заболеваний.
При существующих проблемах с сердечно-сосудистой системой человеку категорически противопоказаны спиртосодержащие напитки. Это чревато мгновенным ухудшением состояния здоровья, возникновением инфарктов и инсультов, и даже смертью. Но и тогда, когда проблем с сосудами человек не испытывает, нагрузка от этанола на них все равно ложится не маленькая. Длительное потребление спиртного приводит к необратимым изменениям – утолщаются сосудистые стенки, нарушается питание сердечной мышцы.
Для быстрого и надежного избавления от алкоголизма наши читатели советуют Препарат "Алкобарьер" . Это натуральное средство, которое блокирует тягу к спиртному, вызывая стойкое отвращение к алкоголю. Кроме того, Алкобарьер запускает восстановительные процессы в органах, которые начал разрушать спирт. Средство не имеет противопоказаний, эффективность и безопасность препарата доказана клиническими исследованиями в НИИ Наркологии. Узнать больше... »В мировом производстве этанол получают химическим путем. Его применяют во всех отраслях народного хозяйства, но до сих пор не утихают споры о том, насколько полезен или вреден этиловый спирт. Для здоровья человека в малых дозах это вещество способно принести пользу – расширить сосуды, улучшить кровообращение, помочь при различных болезнях в виде лекарственных настоек, однако, если этанол применять регулярно, он вызывает привыкание и начинает отравлять организм.
Злоупотребление алкоголем вредно в любом случае, не важно, пьет ли человек дешевую водку или дорогой коньяк. Быстрое распространение по кровеносной системе помогает этиловому спирту проникать во все уголки органов, нарушая их функцию. Вот почему очень важным является умение правильно рассчитывать ту дозу спиртных напитков, которая не приводит к негативным последствиям. Поскольку алкоголь вызывает зависимость, сделать это способен не каждый. Лучше совсем не употреблять этанол в виде спиртного, а применять его в тех областях, где без изобретения этого вещества многих вещей не получилось бы добиться.
Похожие статьи:
Будем признательны, если воспользуетесь кнопочками:
stopalkogolizm.ru