Нитраты - что такое? Нитраты: формула, получение, применение, действие. Нитраты это соли
Нитраты и нитриты. Разложение нитратов. Нитраты в продуктах и воде. Нитраты
Каждый из нас хоть раз в жизни сталкивался с неприятными последствиями употребления продуктов с нитратами. Для кого-то такая встреча продолжилась легким кишечным расстройством, а кто-то умудрился попасть в больницу и еще долгое время с опаской взирал на любые фрукты и овощи, купленные на рынке. Околонаучный подход и недостаточная информированность делают из селитры монстра, способного даже на убийство, однако стоит познакомиться с данными понятиями поближе.
Нитраты и нитриты

Нитриты – это соли азотной кислоты, имеющие вид кристаллов. Они хорошо растворяются в воде, особенно в горячей. В промышленных масштабах их получают при поглощении нитрозного газа. Используются для получения красителей, как окислитель в текстильной и металлообрабатывающей промышленности, как консервант.
Нитраты – это соли азотной кислоты, ранее имевшие название селитры. Их получают после воздействия на металлы азотной кислоты, да и сами по себе они очень сильные окислители. Хорошо растворяются в воде. Разложение нитратов наступает при температуре выше трехсот градусов по Цельсию. Основная область применения нитратов – это сельское хозяйство, но некоторые соединения используют пиротехники в качестве взрывчатых веществ, а также в виде компонентов ракетного топлива.
Роль нитратов в жизни растений
Одним из четырех основных элементов, составляющих живой организм, является азот. Он необходим для синтеза белковых молекул. Нитраты – это молекулы солей, которые содержат необходимое растению количество азота. Поглощаясь клеткой, соли восстанавливаются до нитритов. Последние, в свою очередь, по цепи химических превращений доходят до аммиака. А он, в свою очередь, необходим для образования хлорофилла.
Естественные источники нитратов

Основным источником нитратов в природе является сама почва. Когда органические вещества, которые в ней содержатся, минерализируются - образуются нитраты. Скорость этого процесса зависит от характера землепользования, погоды и вида почвы. В земле не содержится много азота, поэтому экологи не беспокоятся из-за образования значительного количества нитратов. Тем более что сельскохозяйственные работы (боронование, дискование, постоянное использование минеральных удобрений) уменьшают количество органического азота.
Поэтому естественные источники нельзя считать фактором загрязнения подземных вод и накопления нитратов в растениях.
Антропогенные источники

Условно антропогенные источники можно разделить на сельскохозяйственные, индустриальные и коммунальные. К первой категории относятся удобрения и отходы животноводства, ко второй – промышленные сточные воды и отходы производств. Их влияние на загрязнение окружающей среды неодинаково и зависит от специфики каждого конкретного региона.
Определение нитратов в органических материалах дало такие результаты:
- больше 50 процентов – это результат уборочной кампании;- около 20 процентов – навоз;- к 18 процентам приближаются городские коммунальные отходы;- все остальное – это промышленный мусор.
Наиболее серьезный вред наносят азотные удобрения, которые вносятся в почву для увеличения урожая. Разложение нитратов в почве и растениях образует достаточное количество нитритов для пищевого отравления. Интенсификация сельского хозяйства только усугубляет эту проблему. Наиболее высокий уровень нитратов замечают в магистральных водостоках, которые собирают воду после полива.
Воздействие на организм человека
Нитраты и нитриты впервые скомпрометировали себя в середине семидесятых годов. Тогда в Средней Азии врачи зафиксировали вспышку отравлений арбузами. В процессе расследования было выяснено, что фрукты обрабатывали аммиачной селитрой и, видимо, немного перестарались. После этого случая химики и биологи вплотную занялись изучением взаимодействия нитратов с живыми организмами, в частности человеком.
- В крови нитраты взаимодействуют с гемоглобином и окисляют входящее в его состав железо. Так образуется метгемоглобин, который не может переносить кислород. Это приводит к нарушению клеточного дыхания и окислению внутренней среды организма.
- Нарушая гомеостаз, нитраты способствуют росту вредной микрофлоры в кишечнике.
- В растениях нитраты снижают содержание витаминов.
- Передозировка нитратами может привести к прерыванию беременности или к нарушению сексуальной функции.
- При хроническом отравлении нитратами наблюдается снижение количества йода и компенсаторное увеличение щитовидной железы.
- Нитраты – это триггерный фактор для развития опухолей пищеварительной системы.
- Большая доза нитратов одномоментно способна привести к коллапсу из-за резкого расширения мелких сосудов.
Метаболизм нитратов в организме

Нитраты – это производные аммиака, которые, попадая в живой организм, встраиваются в обмен веществ и изменяют его. В небольших количествах они не вызывают беспокойства. С пищей и водой нитраты всасываются в кишечнике, проходят с током крови через печень и выводятся из организма почками. Кроме того, у кормящих матерей нитраты попадают в грудное молоко.
В процессе метаболизма нитраты превращаются в нитриты, окисляют молекулы железа в гемоглобине и нарушают дыхательную цепь. Для того чтобы образовалось двадцать грамм метгемоглобина, достаточно всего одного миллиграмма нитрита натрия. В норме концентрация метгемоглобина в плазме крови не должна превышать пары процентов. Если этот показатель поднимается выше тридцати, наблюдается отравление, если выше пятидесяти – это практически всегда смертельно.
Для контроля над уровнем метгемоглобина в организме есть метгемоглобинредуктаза. Это печеночный фермент, который вырабатывается в организме, начиная с трех месяцев жизни.
Допустимая норма нитратов

Конечно, идеальный вариант для человека – избегать попадания нитратов и нитритов в организм, но в реальной жизни так не бывает. Поэтому врачи санитарно-эпидемиологической станции установили нормы этих веществ, которые не смогут повредить организму.
Для взрослого человека с весом более семидесяти килограмм допустимой считается доза в 5 миллиграмм на килограмм веса. Без серьезных последствий для здоровья взрослый может проглотить до половины грамма нитратов. У детей этот показатель более усредненный – 50 миллиграмм, независимо от веса и возраста. В то же время грудному ребенку для отравления будет достаточно и пятой части от этой дозы.
Пути проникновения

Получить отравление нитратами можно алиментарным путем, то есть через пищу, воду и даже лекарства (если в их состав входят соли нитратов). Больше половины суточной дозы нитратов попадает в человека со свежими овощами и консервами. Оставшаяся доза поступает из выпечки, молочных продуктов и воды. Кроме того, незначительная часть нитратов является продуктами обмена веществ и образуется эндогенно.
Нитраты в воде – это повод для отдельного разговора. Она – универсальный растворитель, следовательно, в ней содержатся не только полезные минералы и микроэлементы, необходимые для нормальной жизнедеятельности человека, но и токсины, яды, бактерии, гельминты, которые являются возбудителями опасных болезней. По данным Всемирной организации здравоохранения, из-за некачественной воды каждый год заболевает около двух миллиардов человек, а умирает из них более трех миллионов.
Химические удобрения, содержащие соли аммония, просачиваются через почву и попадают в подземные озера. Это приводит к накоплению нитратов, и иногда их количество достигает двухсот миллиграмм на литр. Артезианская вода чище, так как добывается из более глубоких слоев, но и в нее могут попасть токсины. Жители сельской местности вместе с колодезной водой ежедневно получают по восемьдесят миллиграмм нитратов из каждого литра выпитой воды.
Кроме того, содержание нитратов в табаке достаточно высоко, чтобы у курильщиков с большим стажем вызвать хроническое отравление. Это еще один довод в пользу борьбы с вредной привычкой.
Нитраты в продуктах

Во время кулинарной обработки продуктов количество нитратов в них существенно снижается, но в то же время нарушение правил хранения может привести к обратному эффекту. Нитриты, наиболее токсичные для человека вещества, образуются при температуре от десяти до тридцати пяти градусов, особенно если место хранения продуктов плохо вентилируется, а на овощах есть повреждения или они начали гнить. Нитриты образуются и в размороженных овощах, с другой стороны, глубокая заморозка предотвращает образование нитритов и нитратов.
При оптимальных условиях хранения можно снизить количество селитры в продуктах до пятидесяти процентов.
Отравление нитратами
Признаки отравления нитратами:
- посинение губ, лица, ногтей;- тошнота и рвота, могут быть боли в животе;- желтушность белков глаз, стул с кровью;- головная боль и сонливость;- заметная одышка, сердцебиение и даже потеря сознания.
Следует помнить, что острое отравление нитратами по своим проявлениям похоже на алкогольную интоксикацию.
Невозможно отделить нашу жизнь от нитратов, потому что это скажется на всех сферах жизни человека: от питания до производства. Однако можно попытаться оградить себя от чрезмерного их потребления, соблюдая простые правила:
- мыть овощи и фрукты перед употреблением;- хранить продукты в холодильниках или в специально оборудованных помещениях;- пить очищенную воду.
fb.ru
это что такое? Реакции нитратов. Растворы нитратов :: SYL.ru
Нитраты большинству людей знакомы в связи с их содержанием в продуктах питания. Но на самом деле они применяются в различных областях промышленности и сельского хозяйства. Об их реакциях, растворах, свойствах, пользе и вреде читайте в статье.
Что такое нитраты?
Это соли азотной кислоты, которые содержат все живые организмы, а также почва, вода. В питательной среде растений содержание нитратов является обязательным. В организм человека их доставляет вода и овощи.
Получение нитратов – результат действия азотной кислоты на такие вещества, как соль, металл, а также гидроксиды и оксиды. Нитраты, в большинстве своем, хорошо растворяются в воде. В растворе нитрата окислительные свойства практически отсутствуют, а вот в твердом состоянии нитраты – сильные окислители. В условиях обычной температуры они обладают устойчивостью. Плавление солей азотной кислоты происходит при температуре 200-600ОС, часто с одновременным разложением.
Нитрат меди
Это вещество неорганического происхождения, соль двухвалентной меди и кислоты азотной. Данный нитрат – это безводное, гигроскопичное вещество с бесцветными кристаллами, но при поглощении ими влаги они приобретают голубой цвет, образуя кристаллогидраты. В природе встречается как минералы: руаит, герхардтит.
Данный нитрат – это вещество, образующее кристаллы твердой консистенции, которые хорошо растворяются в воде и других средах, таких как этанол, этилацетат, метанол и прочих. Нитрат меди применяется в синтезе органических и неорганических соединений. Вещество используется текстильной промышленностью для окрашивания и протравы тканей. В сельском хозяйстве применяется для производства фунгицидов, с помощью которых ведется борьба с заболеваниями грибкового происхождения у растений.
Химические свойства нитрата меди
Данное вещество обладает следующими свойствами:
- Разложением, которое происходит при нагревании нитрата. В результате реакции образуется оксид меди и диоксид азота, который используется для получения кислоты азотной в лабораторных условиях.
- Гидролизом, при котором нитрат меди диссоциирует в воде на ионы.
- Обменными реакциями, в результате которых происходит ионный обмен. Например, если вещество вступает в реакцию со щелочью, выпадает осадок голубого цвета, с фосфатом натрия – синего, с концентрированным аммиачным раствором – темно-синего, с кровяной солью желтого цвета – красного.
Нитрат меди: методы получения
В промышленных условиях соединение получают в результате разложения добытых в природе минералов, таких как руаит, герхардтит. В лабораториях данную методику не используют, так как не позволяют технические условия. Проще будет растворить металлическую двухвалентную медь, ее оксид и гидроксид. Для получения раствора используется нитратная кислота с высокой концентрацией.

Можно получить нитрат меди в результате реакции, для осуществления которой используется металлическая медь и тетраоксид диазот. Важным условием для этого является температура: она должна быть 80ОС.
Барий
Нитрат бария – это соли кислоты азотной, называют азотнокислым барием или бариевой селитрой. Вещество представляет собой негигроскопичные кристаллы без цвета, имеющие кубическую решетку. Растворимо в воде, но при более высокой температуре этот процесс происходит быстрее. В азотной кислоте большой концентрации и спирте не растворяется. Масса нитрата (молярная) составляет 261,337 г/моль, а плотность – 3,24 г/см3. Температура плавления равняется 595ОС. Получают промышленным и лабораторным способами. В природе встречается как минерал нитробарит, который является редким. Его впервые обнаружили в Чили.

Нитрат бария: химические реакции
Это вещество вступает в реакцию со многими соединениями:
- С кислотой серной, в результате чего происходит выпадение сульфата бария в осадок и образование раствора кислоты азотной.
- Если для взаимодействия берется сульфат калия, то в результате реакции образуется его нитрат, а в осадок выпадает сульфат бария.
- Вступает в реакцию с азотной кислотой и сульфатом бария.
- Кислота соляная и нитрат бария никогда не вступают в реакцию.
Нитрат бария: применение
Получение пероксида и оксида бария является основным применением нитратов. Реакции, с помощью которых это происходит, сопровождаются выделением токсичных веществ. Поэтому помещения должны иметь мощную вентиляцию. Пероксид бария используется для производства и отбеливания тканей, бумаги, применяется в составе глазури для изделий из керамики, для ее прочного закрепления. Нитрат бария широко применяется в пиротехнике для получения фейерверков зеленого цвета. Однако важно учитывать, что гигроскопичность вещества небольшая, поэтому для хранения нужны сухие помещения с хорошей вентиляцией. Бариевая селитра, кроме этого, – востребованное вещество для производства взрывчатых материалов.

Работая с реактивом, всегда следует помнить об опасности, подстерегающей человека в случае неправильного обращения с ним. Для азотнокислого бария в помещении для хранения выбирают отдельное место, так как этот нитрат воспламеняется очень легко. Если случится возгорание, пожар следует тушить большим количеством воды.
Нитрат серебра
Это вещество представляет собой кристаллы ромбической формы без цвета. Их внешний вид напоминает пластинки или кристаллические палочки белого цвета без запаха. Нитрат серебра обладает хорошей способностью растворяться в воде и других жидкостях, для этого достаточно 20ОС выше нуля. Его разложение происходит при температуре 300ОС. При воздействии света на него – темнеет. Вещество получают в результате взаимодействия серебра и азотной кислоты. Нитрат, таким образом, является результатом растворения серебра в кислоте.

Фармакологические свойства нитрата серебра
Это вещество обладает следующими свойствами, благодаря которым широко используется в медицине:
- Антисептическими.
- Бактериальными.
- Противовоспалительными.
- Прижигающими.
- Вяжущими.
- Противомикробными.
Нитрат идет на изготовление ляписа. При соприкосновении с кожей на ней появляются пятна черного цвета, а при длительном по времени контакте – ожоги большой глубины. Ляписом в медицине прижигают мелкие раны, трещины, папилломы, наросты, родинки, угри, бородавки. Широкое применение нитрат нашел в стоматологии, гомеопатии и других областях для лечения различных заболеваний.
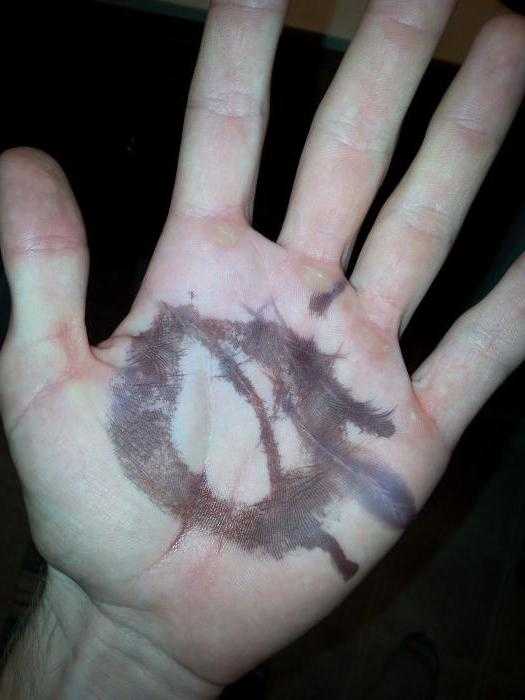
Применение нитрата серебра в прошлом
Адский камень – другое название вещества, с давних пор используется в медицине. Раствор нитрата серебра раньше использовался многими отраслями медицины. Благодаря своим действиям он применялся при лечении язвы желудка. Пациентам назначали раствор в небольших дозах для приема внутрь. Им закапывали глазки новорожденным детям, а также использовали для профилактики гонорейного конъюнктивита у младенцев.
В настоящее время данный раствор используется ограниченно, так как выпускается много других средств, заменяющих его. Но прижигающему свойству препарата и сейчас придается большое значение: им прижигают эрозии, незаживающие раны. Препараты из нитрата серебра чаще всего назначают больным с заболеваниями носа и глотки.
Как производится бариевая селитра?
Существует несколько способов:
- За основу первого метода берется реакция нитрата натрия (селитры) с хлоридом бария. Получается горячий раствор, он остужается, а затем фильтруется и сушится. После этого происходит окисление отфильтрованного материала азотной кислотой. Затем снова осуществляется фильтрация и сушка.
- Основу второго способа составляет применение сульфата бария. Чтобы получить азотнокислый барий, проводят две реакции, а не одну.
- Третий способ применяют в лабораториях. Для получения безводной бариевой селитры удаляют молекулы воды. Сначала осуществляется процесс упаривания раствора, а затем сушки.
Нитраты в организме человека
Нитраты – это такие вещества, чрезмерное содержание которых в организме может вызвать серьезное отравление. Кроме этого, в результате действия микроорганизмов нитраты могут преобразоваться в нитриты. К такому превращению располагает кишечник, особенно при пониженной кислотности. Нитриты взаимодействуют с гемоглобином, в результате чего происходит образование метгемоглобина, не обладающего способностью к переносу кислорода. При такой ситуации наступает кислородное голодание организма. Норма метгемоглобина в крови – 2 %. Если его содержание повысится до 30, наступит сильное отравление, до 50 – смерть.
Нитраты в продуктах питания
Ошибочно считают, что содержанием нитратов богаты только покупные овощи, для выращивания которых использовались различные удобрения. Но это не совсем так. В домашних овощах, для роста и развития которых использовались органические удобрения, нитраты тоже присутствуют. В почву они переходят из навоза или куриного помета, а оттуда – к овощам.

Разные плоды и даже отдельные их части содержат нитраты разной концентрации. Так, например, их больше в кожуре огурцов, в кочерыжке и толстых прожилках капусты, в мякоти дыни или арбуза, расположенной ближе к корке. Внешний вид овоща может быть обманчивым. В крупных, ровных плодах нитратов больше, поэтому лучше выбирать средние по размеру. Если поверхность овоща покрыта уплотнениями, а срез имеет неравномерную окраску, то содержание нитратов в овоще велико. Уменьшить их количество помогает вымачивание и термическая обработка при открытой крышке.
Нитраты содержатся в сырах, колбасах, поэтому частое их употребление приводит к накоплению нитратов. Они выводятся из организма почками, а при грудном вскармливании – молоком матери.
Применение нитратов
Основное применение селитра нашла в сельском хозяйстве. Здесь нитраты используются в качестве удобрений. Азот, который берут растения из соли, необходим им при построении клеток и создании хлорофилла. Кроме этого, из нитратов получают стекло, лекарства. Они идут на производство взрывчатых веществ, пиротехнических средств, компонентов топлива для ракет. Их используют в качестве пищевых добавок при изготовлении колбас и других продуктов.
www.syl.ru
Что такое нитраты и чем они опасны?
Нитраты, или соли азотной кислоты, содержатся в любых продуктах, и в воде. Есть они и в организме человека. И только при повышенной концентрации нитратов появляются отрицательные реакции. Отравление нитратами может сопровождаться тошнотой, одышкой, диареей, а также слабостью и головными болями. В повышенной дозе нитраты могут привести и к изменениям в нервной и сосудистой системах. Особенно чувствительны к нитратам дети, пожилые люди и беременные женщины, а также все, кто страдает заболеваниями сердца. Кстати, нитраты влияют на концентрацию витаминов в овощах, в частности, витамина С. Допустимая доза нитратов составляет чуть более 300 мг в сутки.

ОТКУДА ПОЯВЛЯЮТСЯ НИТРАТЫ?
Причина кроется в химизации растениеводства и условиях выращивания овощей. На концентрацию нитратов влияет и количество солнечного света, и даже густота посева. Кстати, продукты животного происхождения нитратов практически не содержат.
ГДЕ ОНИ СОДЕРЖАТСЯ
Самое «опасное» время – начало уборки урожая. Нитраты может содержать любая зелень: шпинат, щавель, недозрелые овощи. Фрукты, арбузы и дыни содержат наименьшее количество нитратов ввиду большего количества воды в составе. Все овощи можно разделить на три степени опасности по содержанию нитратов.
Высокий: зелень, салаты, ботва свеклы, капуста.
Средний: морковь, белокочанная капуста и огуречные культуры.
Низкий: бобовые, картошка, помидоры.
У каждого растения есть свой участок плода, где могут скапливаться нитраты: в кочане капусты это кочерыжка, в редиске и огуречных культурах – верхний слой, у моркови – серединка, у кабачков, огурцов, дыни – кожура.
ОПРЕДЕЛИТЬ НИТРАТЫ НА ГЛАЗ
Определить количество нитратов в приобретаемых овощах и фруктах на глаз нельзя. Это возможно сделать только при помощи специального прибора.
Справка
Для нейтрализации нитратов необходимо:
- Тщательно мыть овощи и фрукты.
- Вымачивать зеленные культуры.
- Подвергать овощи необходимой тепловой обработке.
- Приобретать овощи и фрукты в сезон плодоношения.
- При консервировании, вымачивании или солении число нитратов уменьшается.
Однако при выборе следует обратить внимание: если размер плода слишком велик, это может свидетельствовать о скоплении вредных солей. Приобретать безопаснее те овощи, которые выращены не в теплицах и в сезон.
КАК ОБЕЗОПАСИТЬСЯ
Чтобы не пришлось промывать желудок и принимать ударную дозу активированного угля, специалисты советуют обращать внимание на фрукты и овощи и по возможности подвергать обработке или вообще не употреблять наиболее «опасные» их части.
Все овощи нужно тщательно мыть и обдавать паром, таким образом можно избавиться от 70 % нитратов. Уменьшается их количество и при хранении.
labuda.blog
Что такое нитраты и чем они опасны
Сейчас очень популярными стали телевизионные передачи, где показывают, как прямо на прилавке проверяют содержание нитратов в овощах и фруктах. Вместе с ведущими программ мы уверены, что высокое их содержание наносит организму вред. Значит, нам пора разобраться, что такое нитраты и чем они опасны при употреблении.
Нитраты — что это такое

Ещё в школе мы проходили неорганические кислоты, одна из них — азотная НNOз, а нитраты — соли этой самой азотной кислоты. Солей азотной кислоты много, а нас будут интересовать лишь те, которыми интересуются растения. Это нитраты аммония Nh5NOз, калия КNOз, кальция Са(NOз)2 и натрия NаNOз: их ещё называют селитрами: аммиачная. натриевая и так далее. Все эти соединения есть в почве, грунтовых водах. плюс ещё попадают туда вместе с удобрениями.
Когда эти нитраты всасываются нашими зелёными друзьями из почвы, воздуха или воды, они идут на образование аминокислот, затем — белков, то есть на строительство органического «тела» растения. Поэтому в растениях нитраты всегда есть. Но если почва содержит их лишком много. то и растение всегда будет содержать их избыток. Ведь азотные удобрения очень хорошо растворяются в воде, значит, есть опасность перекормить ими своих подопечных. Питание всасывается корнями, разносится по сосудам растения, поступает в надземные органы и усваивается постепенно. Теперь становится более понятным, откуда берутся нитраты у овощей, фруктов.
Неестественные источники загрязнения нитратами растений
- Минеральные удобрения, их избыток, который создаётся, когда производитель для наживы использует слишком большие концентрации или количества.
- Применение свежего навоза. Это органическое сильное азотное удобрение. Перед тем, как его добавлять как удобрение. он должен пролежать не менее года в компосте. Если же мы решили применить его свежим, то надо настоять одну часть с одной частью воды в тёплом месте, закрытой ёмкости не менее десяти дней. Затем уже применять для подкормок-поливов, разбавив 1:10 с водой.
- Сточные воды от различных производств. Они плохо очищаются, засоряют грунтовые воды, далее используются для полива.
Какие факторы влияют на накопление нитратов
- Плохая освещённость растущих овощей. Даже на одной грядке, если она по-разному освещена, содержание селитры будет разным. Высокая плотность, загущенность посевов здесь на первом месте.
- Высокая кислотность означает увеличение количества нитратов.
- Засуха, недополив провоцируют накопление большого количества нитратов у растения.
- Конкретная биологическая особенность выращиваемой культуры.
- Совместное внесение фосфора. но это не всегда так.
- Недостаток определённых микроэлементов, являющихся катализаторами преобразования нитратов, например, молибдена.
Не всегда нам даже на своих участках удаётся соблюсти баланс между перечисленнымифакторами, что уж говорить об огромных полях с овощами и их владельцах, где прибыль рулит.
Чем опасны нитраты
Сами по себе они не опасны. Но уже в растениях, а затем организме человека при поедании продукта, содержащего нитраты, происходит восстановление их до нитритов, то есть они начинают переходить в соли азотистой кислоты HNO2, имеющими высокую токсичность.
Если почки человека работают хорошо, он пьёт достаточное количество чистой воды, избыток селитры при разумной концентрации выведется из организма без последствий. Но при разных нарушениях деятельности пищеварительного тракта, особенно при низкой кислотности бактерии кишечника переведут нитраты в нитриты. Далее, их взаимодействие с гемоглобином крови приведёт к кислородному голоданию, так как эритроциты не смогут доставлять кислород клеткам организма. Также нитриты, если еда богата белками, образуют опасные соединения нитрозамины и нитрозамиды, являющиеся канцерогенами.
Вот в чём состоит вред нитратов для организма человека.
Если растение полностью усвоит нитраты, нам бояться нечего, так как и нитритам неоткуда взяться.
Поэтому Важное значение имеет условия выращивания: свет. тепло, микроэлементы, углекислый газ для дыхания, необходимый полив.
Где нитратов больше, в каких частях овощей и фруктов
Во фруктах их содержится гораздо меньше, чем овощах и зелени. Причём в разных частях разное количество. Недозрелые плоды всегда имеют их больше, потому что ещё идёт процесс питания и созревания.
Морковь — почти все селитры у сердцевины, а также ближе к листовой розетке; натёртаяморковь, если там есть нитраты, опасна быстрым их переходом в нитриты.

Свекла — максимальное количество содержится там, где росла ботва и в хвостике.

Картофель — опасен близкий к кожуре слой мякоти; надо замочить холодным раствором соли с концентрацией 1%.
Капуста — максимум в кочерыжке и листовых утолщениях. Если капусту квасят, надо подождать несколько дней, чтобы нитраты перешли в рассол. А я маленькой всегда ела кочерыжки, вкусно!
Баклажаны — больше рядом с плодоножкой.
Редис — опасны кожура, верхушки, хвостики.
Томаты — верхняя часть у плодоножки.

Зелёный лук — около корня.
Перчик — у плодоножки.
Арбузы, дыни — на границе мякоти с коркой.
Огурцы, кабачки — кожура и кончики. ранние плоды лучше очистить от кожурки.
Укроп, другие зеленные — стебли и утолщения.
Яблоки, груши, если купили, да ещё импортные. лучше очистить от кожуры.
Разные растения накапливают разное количество нитратов. например, помидоры, баклажаны, зелёный горошек, фасоль, лук репчатый много нитратов не могут накопить, тогда как свекла, редька, укроп, петрушка, листовой сельдерей, пекинская капуста — рекордсмены по их содержанию.В злаковых нитратов нет, они остались в зелёных частях.
Нитраты в овощах — признаки
- Их больше у крупных плодов, если только это не сортовой признак. Вес и объём им нагоняют усиленными подкормками и стимуляторами.
- Подозрительно выровненые размеры.
- Отсутствие сладости у плода, сладкого по определению (например, дыня, арбуз).
- Наличие уплотнений, нехарактерная более светлая окраска прожилок, концентрических кругов.
- Отсутствие должного аромата.
- Семена не вызревшие.
- В тепличных зимних овощах нитратов всегда больше, потому тепличный огурец в разрезе желтоватый на цвет, скользкий на ощупь, неприятный на вкус.
Симптомы отравления нитратами
Признаки появляются уже через 4-6 часов.
- тошнота
- головокружение
- диарея
- рвота
- головная боль
- большая слабость
- боли печени и желудка
- сильно повышается температура
Лечение и первая помощь
При отравлении надо выпить 500 мл розового раствора марганцовки, вызывая рвоту. Затем принять 8-10 таблеток активированного угля. В состоянии покоя пить тёплый крепкий сладкий чай с лимоном. Всё должно наладиться. Если отравление сильное, лучше вызвать скорую.
Как нейтрализовать вред нитратов
- Листовую зелень, корнеплоды перед употреблением замочить в холодной воде на полчаса.
- Не употреблять для еды ранние тепличные овощи и зелень.
- Лимоны и гранаты обезвреживают нитраты. можно добавлять их в салаты.

- Перед употреблением срезать у овощей и фруктов те части. где нитратов больше всего.
- Кожицу ранних овощей, например, молодого картофеля. счищать.
- Варка, приготовление на пару, жарка — всё это снижает количество нитратов.
- Если сомневаетесь в продукте, но очень хочется его съесть, примите до еды аскорбинку — она не даст образоваться опасным соединениям.
- Замороженные овощи и фрукты надо переработать без медленного размораживания.
- Увядающие зелень и фрукты с овощами тоже накапливают нитраты, вернее, они переходят в нитриты.
- Покупаем плоды средних размеров, неповреждённые, зрелые.
- При покупке зелени поставьте её в воду не менее чем на час, не измельчайте, чтобы не образовывались нитриты.
- Заправляйте салаты маслами, они сдерживают образование опасных нитритов.

- Для приготовления соков овощи и фрукты надо вымочить минут 20, выжать и сразу выпить.
Приятного аппетита и будьте здоровы!
Как определить нитраты в овощах в домашних условиях:
Возможно, Вас заинтересует следующая информация:
vosadyli.ru
что такое? Нитраты: формула, получение, применение, действие
Среди информации, посвященной проблеме правильного питания, можно выделить сегмент, раскрывающий влияние на организм человека таких веществ, как нитраты. Действие их на наше здоровье неоднозначно. Как не вспомнить известное выражение Парацельса: «Всё есть яд и всё есть лекарство; тем или иным его делает только доза». Действительно, для правильного обмена веществ необходимо присутствие в цитоплазме клеток анионов NO3- NO4+. В то же время избыток соединений, содержащих эти ионы, в продуктах питания опасен для здоровья человека. Роль солей азотной кислоты, их получение, применение нитратов будут рассмотрены в данной статье.
Положение нитратов в классификации неорганических веществ
Многие знают, что соли азотной кислоты, хорошо растворимые в воде – это нитраты. Что такое селитра, известно не всем. Оказывается, так ранее в химии называли особые вещества – соли нитратной кислоты. До сих пор мы можем слышать этот термин применительно к химии минеральных удобрений. В селитрах нитрат-ион связан с катионами калия, кальция, натрия и аммония. Они представляют собой средние соли. Оказалось, что нитраты натрия, калия и другие соли при нагревании разлагаются, причем продукты реакции зависят от того, какой катион входит в состав молекулы. Так, нитраты, формула которых KaNO3 илиNaNO3, термически разлагаются до соответствующего нитрита и свободного кислорода, а азотнокислый магний при нагревании образует оксид, двуокись азота и кислород.

Получение нитратов
Основной способ – переработка природных минералов, содержащих соли азотной кислоты. Так, чилийская селитра, представляющая собой минерал нитронатрит, – один из главных источников их получения. На заводах туковой промышленности горную породу, содержащую нитрат натрия, мелко измельчают и в расфасованном виде поставляют сельхозпредприятиями фермерского хозяйства в качестве азотного удобрения. Применяют его прежде всего для прироста вегетационной массы овощных, зерновых и плодово-ягодных культур, а также для повышения их урожайности. В лабораторных условиях соли азотной кислоты получают реакцией обмена между щелочами и нитратной кислотой или же взаимодействием металлов с концентрированной HNO3. Применение азотных удобрений, таких как калийная селитра, нитрат аммония, – необходимое условие для получения стабильных высоких урожаев основных сельскохозяйственных культур.
Агротехнические условия внесения азотных удобрений (нитратов)
К ним относят прежде всего соблюдение норм внесения препаратов в почву. Например, для аммиачной селитры, содержащей до 35 % азота, допустимая норма составляет не более 25 г на один квадратный метр. Кальциевая селитра, в которую входит до 15,5 % азота, вносится из расчета до 50 г на 1 м. Нарушение агротехнических норм азотной подкормки растений приводит не только к загрязнению почвы и снижению её восстановительной функции, но и к опасной концентрации таких соединений, как нитраты, в овощах и фруктах. На этом вопросе мы остановимся далее.

Как нитраты попадают в растения
Рассмотрим, какими именно путями поступают в почву нитраты, что такое допосевное внесение, стартовое удобрение и подкормка. В сельском хозяйстве основное внесение удобрений проводят весной и при этом обращают внимание на состав почвы и особенности климата. Цель – обеспечение азотного питания в период вегетации растения.

При использовании стартового способа селитру вносят непосредственно в ряды или лунки, используя нитраты в минимальных дозах, чтобы «не обжечь» хрупкие корни высаживаемой рассады. Подкормка осуществляется во время наиболее интенсивного поглощения растениями питательных элементов. Её проводят в форме вегетирующих культур или как корневую подкормку растворами нитратов. В почвенном субстрате ионы аммония или нитрат ионы путем диффузии легко поглощаются корневыми волосками и далее поступают в ксилему. Из нее состоят проводящие элементы растений. У голосеменных это трахеиды, а у цветковых – сосуды (трахеи). Атомы азота, входящие в состав нитратов, включаются в цикл Кальвина, осуществляемый в темновой фазе фотосинтезом, и в дальнейшем входят в состав синтезируемых аминокислот и далее в растительные белки.
Чем опасно избыточное содержание солей нитратной кислоты
Если концентрация вышеназванных соединений превышает допустимую норму, это может определить прибор для измерения нитратов в продуктах. Он доступен в продаже и используется во многих семьях, ответственно относящихся к своему здоровью. Исследования медицины доказали, что избыток солей HNO3 в желудочно-кишечномтракте превращается в нитриты. Именно они вызывают раздражение слизистых оболочек желудка и двенадцатиперстной кишки, симптоматически проявляющиеся явлениями диспепсии и пищевого отравления. Также установлено, что избыток солей HNO2 плохо выводиться почками, поэтому они накапливаются в почечной паренхиме. Известно, что сами почки играют ведущую роль в метаболизме и выведении вредных продуктов обмена. Снижение фильтрационной функции почек является очень опасным осложнением, возникающим в результате отравления солями азотной и азотистой кислот. В результате употребления продуктов с высоким содержанием нитратов страдает также и печень, являющаяся еще одним детоксикационным органом. Ее повреждение нитратами чревато тяжелыми повреждениями вплоть до перерождения гепатоцитов в жировую ткань.

Кислородное голодание тканей как последствие их отравления нитратами
Питательные вещества (жиры, углеводы) могут сохраняться в качестве запасного источника энергии и расходуются организмом постепенно. Именно поэтому человек способен в течение 5-7 дней обходиться без пищи. Но кислород, в отличие от углеводов и жиров, не может длительно сохраняться в клетках или тканях, поэтому гипоксия в течение 5-15 минут приводит к гибели сначала клеток головного мозга, а затем и всего организма человека в целом. Кажущиеся на первый взгляд безобидными, нитраты в фруктах, овощах, молочных детских смесях способны вызывать разрушение дыхательных цепей в митохондриях, нарушать образование связи пигмента эритроцитов – гемоглобина – с молекулами кислорода.

И препятствовать его переносу к органам и тканям. Поэтому избыточная концентрация в цитозоле клетки таких соединений, как нитраты (формула - Me(NO3)N1), может привести к серьезным нарушениям функций со стороны таких физиологических систем, как пищеварительная, выделительная, а также нервная.
Какие продукты могут быть загрязнены солями нитратной кислоты
У большинства людей избыточное содержание этих веществ ассоциируется с овощами или фруктами, например арбузом, картофелем, редисом или клубникой. Но оказывается, что загрязнение почвы и особенно воды азотными удобрениями, попавшими туда в связи с нарушением норм их внесения, напрямую влечет за собой «оседание нитратов» в организмах домашних животных. Поэтому бесконтрольное и нерациональное применение нитратов влечет за собой их высокое содержание в продуктах животноводства: мясе, молоке и даже в меде. Опрыскивание растений-медоносов (гречихи, рапса) растворами солей азотной кислоты в качестве жидкого удобрения приводит к появлению токсинов и в продуктах пчеловодства.

Как определить содержание солей азотной кислоты в продуктах
Давайте уточним, как же практически можно узнать о концентрации в пищевых веществах таких соединений, как нитраты. Что такое нитрат-тестер, рассмотрим более подробно. Чтобы выявить присутствие солей азотной кислоты, нужно погрузить щуп прибора в мякоть арбуза или другого продукта. Приспособление имеет две части: положительно и отрицательно заряженную. А сам нитратомер определяет электропроводность раствора клеточного сока. Полученные результаты сравниваются с ПДК исследуемого продукта, и прибор для измерения нитратов в продуктах выводит на дисплей результат с содержанием солей в мг/кг. Особенно желательным будет тестирование пищевых продуктов, используемых в питании маленьких детей, беременных и кормящих женщин, а также людей, страдающих хроническими заболеваниями ЖКТ и почек.

Отравление солями нитратной кислоты и его профилактика
Пик регистрируемых случаев интоксикаций, связанных с отравлениями солями азотной кислоты, проходится на конец зимы – начало весны. Вследствие дефицита солнечного света и энергии, человеческий организм в этот период остро нуждается в витаминах, содержащихся в свежих овощах и фруктах. Поэтому в супермаркетах не залеживаются тепличные огурцы, помидоры, пряно-вкусовые приправы (сельдерей, петрушка, укроп), а также клубника. Агротехнологии их выращивания предусматривают обязательное применение таких веществ, как нитраты. Что такое минеральные удобрения и как их избыток влияет на организм человека, было уже рассмотрено нами ранее. Сейчас мы остановимся на приемах первой помощи, способных облегчить состояние больного с симптомами отравления нитратами. В первую очередь нужно вызвать рвоту, чтобы удалить из желудка токсичный продукт. Для этого применяют обильное питье. Затем принимают препараты-энтеросорбенты и продолжают соблюдать водно-солевой режим. При сложных симптомах, таких как падение кровяного давления, потеря сознания, судороги, вызванных поражением центральной нервной системы и почек, следует срочно вызвать "скорую помощь".
fb.ru
нитраты - это... Что такое нитраты?
НИТРА́ТЫ -ов; мн. (ед. нитра́т, -а; м.). [от греч. nitron - селитра]
1. Хим. Соли и эфиры азотной кислоты (применяются в технике, в медицине). // Азотнокислые соли аммония и некоторых металлов; селитры (широко применяются в качестве минеральных удобрений). / только мн. Разг. О содержании таких солей в злаках, овощах, фруктах, превышающем допустимые нормы. Н. очень вредны для здоровья. Свёкла с нитратами.
НИТРА́ТЫ, соли азотной кислоты (см. АЗОТНАЯ КИСЛОТА) HNO3, твердые хорошо растворимые в воде вещества. Традиционное русское название некоторых нитратов щелочных и щелочноземельных металлов и аммония — селитры (см. СЕЛИТРЫ) (аммонийная селитра Nh5NO3, калийная селитра КNO3, кальциевая селитра Са(NO3)2 и др. Нахождение в природе и получение Нитрат натрия NаNO3 (чилийская селитра) и нитрат калия КNO3 (индийская селитра) встречаются в природе в Индии и в Чили. В России натриевую селитру в виде белого налета получали при гниении различных органических остатков растительного и животного происхождения. Так как нитрат натрия гигроскопичен и не годится для изготовления пороха, его превращали в нитрат калия обработкой горячим насыщенным раствором КСl. В настоящее время нитраты натрия и калия получают при нейтрализации азотной кислоты с использованием соды Na2CO3, поташа K2CO3 и др. Химические свойства Нитраты характеризуются сильным окислительным действием, они входят в состав горючих смесей, прежде всего черного пороха: 2КNO3 + S = SO2 + KNO2Нитрат аммония используют как компонент твердого ракетного топлива. При сильном (выше 500—600°C) нагревании нитраты щелочных металлов разлагаются с выделением кислорода: 2NаNO3 = 2NаNO2 + O2или с выделением кислорода и диоксида азота: 6КNO3 = 2К3NO4 + 4NO2 + О2Разложение нитратов переходных металлов происходит с образованием соответствующего оксида металла, например: 2Pb(NO3)2 = 2PbO + 4 NO2 + O2Если при этом металл имеет низкую химическую активность и его оксид нестабилен при нагревании, то при разложении образуется сам металл, например: 2AgNO3 = 2Ag + 2NO2 + O2 Физиолгическое действие Нитраты токсичны. Неорганические нитраты вызывают отек легких, тошноту, рвоту, острую сердечно-сосудистую недостаточность. Смертельная доза для человека 8—15 мг/л, допустимое суточное потребление 5мг/л. Для суммы нитратов Na, K, Ca, Nh5 Пдк: в воде 45 мг/л, в почве 130 мг/кг, в овощах и фруктах (мг/кг): картофель 250, капуста белокочанная поздняя500, морковь поздняя 250, свекла 1400, лук репчатый 80, кабачки 400, дыни 90, арбуз, груши, яблоки 60. Вдыхание паров органических нитратов, попадание их на кожу и в пищеварительный тракт вызывает головную боль, учащенное сердцебиение. Окисляют гемоглобин в метгемоглобин. Применение Нитраты аммония, натрия и калия широко применяют как минеральные азотные удобрения. Так как нитраты хорошо растворимы в воде, то после внесения этих удобрений в почву они быстро оказываются в растениях. Поэтому существует опасность избыточного содержания нитрат-ионов в плодах.dic.academic.ru
Нитраты
Нитраты — соли азотной кислоты HN03 — являются нормальным продуктом обмена азотистых веществ любого живого организма, растительного и животного. Поэтому «безнитратных» продуктов в природе не бывает. Даже в организме человека в сутки образуется и используется в обменных процессах 100 мг и более нитратов.
Опасность нитратов
Но почему же говорят об опасности нитратов? При потреблении их в повышенных количествах (о допустимом пределе содержания в рационе нитратов — чуть позже) нитраты в пищеварительном тракте частично восстанавливаются до нитритов (более токсичных соединений), а последние при поступлении в кровь могут вызвать метгемоглобинемию. Кроме того из нитритов в присутствии аминов могут образоваться N-нитрозамины, обладающие канцерогенной активностью (т. е. способствуют образованию рака). При приеме высоких доз нитратов с питьевои водой или продуктами через 4—6 ч появляется тошнота, одышка, посинение кожных покровов и слизистых, понос. Сопровождается все это общей слабостью, головокружением болями в затылочной области, сердцебиением. Первая помощь — обильное промывание желудка, прием активированного угля, солевых слабительных, свежий воздух.
Какова безопасная доза нитратов?
Допустимая суточная доза нитратов для взрослого человека составляет 325 мг в сутки. Как известно, в питьевой воде допускается до 45 мг/л нитратов. Рекомендуемое потребление продуктов питания, где используется питьевая вода (чай, первые и третьи блюда) примерно 1,0—1,5 л, максимум 2,0 л в день. Таким образом, с водой взрослый может потребить около 68 мг нитратов. Следовательно, на пищевые продукты остается 257 мг нитратов. Исследования показали, что токсическое действие нитратов в пищевых продуктах проявляется слабее чем содержащихся в питьевой воде, примерно в 1,25 раза, т. е. фактически безопасно с пищевыми продуктами потреблять 320 мг нитратов в сутки.
В каких продуктах содержатся нитраты?
Каковы же основные источники пищевых нитратов? Практически, это исключительно растительные продукты. Животные продукты (мясо, молоко) их содержат, как правило очень мало. Поскольку нитраты, как отмечалось выше являются нормальным продуктом обмена азота в растениях, то они максимально накапливаются в период наибольшей активности их созревания.
Чаще всего она проявляется перед началом уборки урожая. Поэтому недозрелые овощи (кабачки, баклажаны) и картофель, а также овощи раннего созревания могут содержать нитратов больше, чем достигшие нормальной уборочной зрелости. Кроме того, содержание нитратов в овощах может резко увеличиться при неправильном применении азотистых удобрений (не только минеральных, но и органических). Например, внесение их незадолго до уборки.
У различных растений есть и свои индивидуальные особенности накопления нитратов. Есть и «накопители» нитратов. К ним относятся зеленые листовые овощи: салат, ревень, петрушка, шпинат, щавель, которые могут накапливать до 200—300 мг % нитратов. Свекла может накапливать до 140 мг % нитратов (это предельно допустимая концентрация), а некоторые сорта и больше, другие овощи — значительно меньше (мг %): картофель до 25, ранняя морковь — до 40, поздняя — до 25, кабачки — до 40, огурцы — до 15, капуста белокочанная ранняя — до 90, поздняя — до 50. Фрукты, ягоды и бахчевые содержат нитратов очень мало (меньше 10 мг %). В растениях нитраты распределены неравномерно. В капусте, например, нитраты больше всего накапливаются в кочерыжке, в огурцах и редисе — в поверхностных слоях, в моркови — наоборот. В среднем при мойке и зачистке овощей и картофеля теряется 10—15% нитратов. Еще больше — при тепловой кулинарной обработке, особенно при варке, когда теряется от 40% (свекла) до 70% (капуста, морковь) или 80 % (картофель) нитратов.
Поскольку нитраты довольно химически активные соединения то при хранении овощей их содержание уменьшается: за несколько месяцев на 30—50%.
Реальная опасность нитратов для здоровья
Теперь, когда все известно о пищевых нитратах, попробуем представить их реальную опасность для здоровья. Рассмотрим основные источники нитратов. Начнем с зеленых овощей (салат, петрушка, укроп и т. д.). Их потребление практически редко превышает 100 г в день, а чаще всего около 50 г, т. е. с одной порцией можно получить менее трети от безопасной суточной дозы. Выше отмечалось, что с учетом биоэквивалента безопасная доза нитратов в пищевых продуктах составляет около 320 мг. Теперь перейдем к свекле. Ее, как известно, потребляют только в отварном виде. Так как при варке (40%) и зачистке (10%) теряется половина нитратов, а общественное питание рекомендует порцию отварной свеклы в 125 г, то со свеклой мы можем получить лишь 100 мг нитратов (меньше трети суточной дозы). Картофель и капуста в отварном виде потребляются порциями по 300 г. С учетом потерь при зачистке и кулинарной обработке с одной порцией этих продуктов можем потребить около 60 мг нитратов.
Аналогичные расчеты были сделаны и по остальным овощам и другим продуктам, которые показали, что при обычном рациональном потреблении овощей в свежем или обработанном виде мы с пищевыми продуктами практически никогда не сможем превысить безопасную суточную дозу нитратов. Тем более, что в соответствии с рекомендациями по рациональному питанию не следует постоянно питаться одними и теми же продуктами, например картофелем или капустой. Действительно, если обратиться к рекомендуемому рациональному среднему суточному набору продуктов, то картофеля следует потреблять 265 г (в расчете на покупной продукт), овошей и бахчевых — 450 г (включая 100 г капусты). Такой рацион может дать нам максимум — 200 мг нитратов. Практически же, как показали расчеты, среднесуточное поступление нитратов с основными корнеплодами, овощами, бахчевыми и фруктами с учетом данных фактического питания и фактического содержания нитратов в пище не превышает 100 мг. При этом примерно треть нитратов попадает со свеклой, чуть меньше — с капустой и картофелем, на остальные овощи и фрукты — менее 10%. Если же нарушать принципы рационального питания, например питаться одними овощами, да еще сырыми, как это рекомендуют некоторые поклонники вегетарианства и сыроедения (до 1,5 кг сырых овощей в день), то тут действительно можно превзойти безопасную дозу нитратов почти в 2 (более 650 мг в сутки) раза, на что мы и обращаем внимание.
См. также: Есть ли какая-нибудь специальная «живая» энергия в сырых продуктах?
Для дополнительной безопасности не лишне вспомнить второй принцип рационального питания, предусматривающий необходимость разнообразия пищи. Поэтому не рекомендуем постоянно потреблять, да еще три раза в день, на закуску один и тот же овощ, например одну свеклу. Ограничивать же использование овощей и фруктов в питании из-за опасности нитратного отравления не следует, это лишит нас так необходимых нам витаминов.
Тем более, что благодаря тревоге общественности сейчас устанавливается строгий контроль в местах производства овощей и на торговых базах.
Итак, не бойтесь нитратов, но не злоупотребляйте чрезмерным потреблением сырых овощей.
dietolog.org