Тема Кислоты Определение это сложные вещества. Определение сложное вещество
Вещество. Строение вещества. Простые и сложные вещества.
Насколько я знаю, Вещество - это то, из чего состоит тело. Пример: резина-вещестро, резиновый мячик-тело. Строение вещества. Вещество состоит из молекул, а молекулы состоят из атомов. Простые вещества состоят из атомов одного элемента. Например, кислород, водород, хлор и железо - простые вещества. Сложные вещества состоят из атомов разных элементов. Например, вода - она состоит из двух атомов элемента водорода и из одного атома элемента кислорода. Я СПИСАЛА ИЗ УЧЕБНИКА!! ! =)
по нашему: 1вещество это енергия определеной структуры и степени сжатия: пример, водород-степень сжатия равна 1-е, пара зарядов, гелий это то же, только в два раза более мощно 2однородая масса (заряды) 3разнородная масса
простые вещества состоят из атомов элементы которых одинаковы : h3.Cl2 Mn и так далее сложные вещества включают в себя 2 и более разных элементов : h3O HNO3. AL2(SO4)3 вещество это то из чего состоят тела.
Вещество-это то, что действует на наши органы чувств те или иные ощущения. По элементному составу различают простые вещества, состоящие из атомов одного элемента (h3, O2, Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (h3O, Nh4, OF2, h3SO4, MgCl2, K2SO4).Простые делятся на металлы и неметаллы. Сложные делятся на оксиды, основания, кислоты и соли. Свойства вещесва: физические (описание внешних признаков вещества) и химические (превращения вещества)
1вещество это енергия определеной структуры и степени сжатия: пример, водород-степень сжатия равна 1-е, пара зарядов, гелий это то же, только в два раза более мощно 2 Однородая масса 3 Разнородная масса Ну в роди всё написал )
спасибо огромное всем
touch.otvet.mail.ru
Сложные вещества | Химическая энциклопедия

Химические элементы существуют не только в виде свободных атомов и простых веществ. Они также могут входить в состав самых различных химических соединений. Сложные вещества — это вещества, состоящие из атомов разных химических элементов.
Подавляющее большинство химических веществ – это сложные вещества. Вода, метан, сахар, поваренная соль – простейшие примеры сложных веществ. Сложные вещества делятся на две группы – неорганические и органические. Все органические вещества объединяет главный признак – в их состав обязательно входят атомы углерода. Кроме углерода, в состав органических веществ чаще всего входят атомы водорода, кислорода, а также азота, фосфора, серы. Почти все органические вещества горючи и легко разлагаются при нагревании. Практически все они имеют молекулярное строение.
Простейшим органическим веществом является природный газ метан. Органических веществ миллионы. Они содержатся во всех животных и растительных организмах (откуда и произошло их название), входят в состав пищи, топлива, лекарств, красителей, самых разнообразных материалов.
Неорганические вещества являются соединениями атомов всех остальных элементов, кроме углерода. К неорганическим традиционно относят также несколько веществ, содержащих углерод: углекислый и угарный газы, мел, соду и т.п.
Неорганических веществ около 500 тыс., но масса их многократно превышает массу органических веществ. Почти все они – твердые вещества немолекулярного строения, входят в состав минералов, почв, горных пород. Вам необходимо включить JavaScript, чтобы проголосовать
abouthist.net
Тема Кислоты Определение это сложные вещества
 Тема «Кислоты»
Тема «Кислоты»
 Определение • это сложные вещества, состоящие их ионов водорода и кислотного остатка. Н CL
Определение • это сложные вещества, состоящие их ионов водорода и кислотного остатка. Н CL
 Названия распространенных кислот • • • • HCl - хлороводородная (соляная) HF - фтороводородная (плавиковая) HBr - бромоводородная HI - йодоводородная H 2 S - сероводородная H 2 CO 3 - угольная H 2 SO 4 - серная H 2 SO 3 - сернистая HNO 3 - азотная HNO 2 - азотистая H 3 PO 4 - ортофосфорная HCl. O - хлорная HCN – синильная
Названия распространенных кислот • • • • HCl - хлороводородная (соляная) HF - фтороводородная (плавиковая) HBr - бромоводородная HI - йодоводородная H 2 S - сероводородная H 2 CO 3 - угольная H 2 SO 4 - серная H 2 SO 3 - сернистая HNO 3 - азотная HNO 2 - азотистая H 3 PO 4 - ортофосфорная HCl. O - хлорная HCN – синильная
 Классификация кислоты Бескислородные H 2 S, HCL Одноосновные HNO 3, HCL Кислородсодержащие H 2 SO 4, HNO 3 , H 2 CO 3 Двухосновные H 2 SO 4 , H 2 CO 3 Трехосновные H 3 PO 4
Классификация кислоты Бескислородные H 2 S, HCL Одноосновные HNO 3, HCL Кислородсодержащие H 2 SO 4, HNO 3 , H 2 CO 3 Двухосновные H 2 SO 4 , H 2 CO 3 Трехосновные H 3 PO 4
 Кислоты в нашей жизни Муравьиная Уксусная Сахарная Яблочная Щавелевая Лимонная Молочная Винная Салициловая
Кислоты в нашей жизни Муравьиная Уксусная Сахарная Яблочная Щавелевая Лимонная Молочная Винная Салициловая
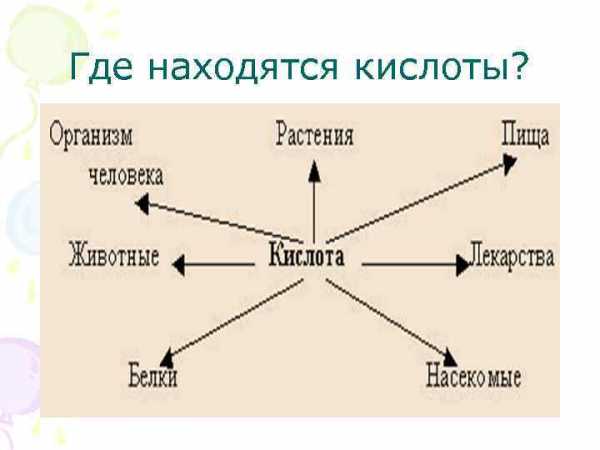 Где находятся кислоты?
Где находятся кислоты?
 Самые важные кислоты H SO -серная кислота тяжелая маслянистая жидкость, сильный окислитель, электролит. 2 4 Издавна её называют «матерью всех кислот» , «Купоросное масло»
Самые важные кислоты H SO -серная кислота тяжелая маслянистая жидкость, сильный окислитель, электролит. 2 4 Издавна её называют «матерью всех кислот» , «Купоросное масло»
 Разбавление серной кислоты водой • С давних пор существует строгое правило: «Сначала вода, потом кислота, иначе случится большая беда!» • Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
Разбавление серной кислоты водой • С давних пор существует строгое правило: «Сначала вода, потом кислота, иначе случится большая беда!» • Если же сделать наоборот, то первые же порции воды, оставшись наверху (вода легче кислоты) и взаимодействуя с кислотой, разогреваются так сильно, что вскипают и разбрызгиваются вместе с кислотой; могут попасть в глаза, на лицо и одежду.
 Алхимикам удалось получить серную кислоту еще в X веке при прокаливании солей - сульфатов (купоросов). Отсюда произошло историческое название серной кислоты – купоросное масло.
Алхимикам удалось получить серную кислоту еще в X веке при прокаливании солей - сульфатов (купоросов). Отсюда произошло историческое название серной кислоты – купоросное масло.
 Самые важные кислоты • HNO 3 -азотная кислота Бесцветная летучая жидкость с резким запахом, дымит на воздухе, сильный окислитель. Её называют «царицей всех кислот» Она необходима для взрывчатых веществ, для красителей, лаков, лекарств. Фотопленка, целлулоид, полимеры, удобрения – вот ее применение.
Самые важные кислоты • HNO 3 -азотная кислота Бесцветная летучая жидкость с резким запахом, дымит на воздухе, сильный окислитель. Её называют «царицей всех кислот» Она необходима для взрывчатых веществ, для красителей, лаков, лекарств. Фотопленка, целлулоид, полимеры, удобрения – вот ее применение.
 Самые важные кислоты • HCl – соляная (хлороводородная кислота) Соляная кислота входит в состав желудочного сока • В желудке она активирует фермент пепсиноген, разлагающий чужие белки, попавшие с пищей, на составные части.
Самые важные кислоты • HCl – соляная (хлороводородная кислота) Соляная кислота входит в состав желудочного сока • В желудке она активирует фермент пепсиноген, разлагающий чужие белки, попавшие с пищей, на составные части.
 Биологическая роль соляной кислоты • Соляная кислота - сильный бактерицид. Большинство бактерий, попавших в желудок с пищей, погибают под ее действием. Так что врачи не случайно тревожатся, если у пациента пониженная кислотность желудочного сока. • Если воспалительные процессы в желудке больного человека проходят на фоне повышенной кислотности, раковых поражений, как правило, не бывает. • Интересно, что у птиц, питающихся падалью, кислотность желудочного сока огромна. И это помогает им расправляться с теми миллиардами микробов, которые буквально кишат в падали.
Биологическая роль соляной кислоты • Соляная кислота - сильный бактерицид. Большинство бактерий, попавших в желудок с пищей, погибают под ее действием. Так что врачи не случайно тревожатся, если у пациента пониженная кислотность желудочного сока. • Если воспалительные процессы в желудке больного человека проходят на фоне повышенной кислотности, раковых поражений, как правило, не бывает. • Интересно, что у птиц, питающихся падалью, кислотность желудочного сока огромна. И это помогает им расправляться с теми миллиардами микробов, которые буквально кишат в падали.
 Самые важные кислоты Уксусная кислота - самая древняя. Упоминания о ней содержатся в древнейших рукописях. Впервые она получена из виноградного сока. Из всех кислот она конечно, прима Присутствует везде и зримо и не зримо. В животных и в растеньях есть она Всем известный “аспирин” - он как добрый господин, жар больного понижает и здоровье возвращает!”
Самые важные кислоты Уксусная кислота - самая древняя. Упоминания о ней содержатся в древнейших рукописях. Впервые она получена из виноградного сока. Из всех кислот она конечно, прима Присутствует везде и зримо и не зримо. В животных и в растеньях есть она Всем известный “аспирин” - он как добрый господин, жар больного понижает и здоровье возвращает!”
 Самые важные кислоты HF – Фтороводородная кислота (плавиковая) • Плавиковая кислота обладает оригинальными свойствами: она легко реагирует со стеклом и химически растворяет его, поэтому хранить кислоту приходится не в стеклянной посуде, а в полиэтиленовой. • Представьте, что получится, если какой-то химик перельёт эту кислоту в стеклянную колбу !
Самые важные кислоты HF – Фтороводородная кислота (плавиковая) • Плавиковая кислота обладает оригинальными свойствами: она легко реагирует со стеклом и химически растворяет его, поэтому хранить кислоту приходится не в стеклянной посуде, а в полиэтиленовой. • Представьте, что получится, если какой-то химик перельёт эту кислоту в стеклянную колбу !
 Кислоты в природе • Кислоты постоянно присутствуют вокруг нас. Например, дождевая вода на первый взгляд кажется чистой. На самом деле в ней присутствует немало других веществ. За счет растворения углекислого газа из атмосферы она является раствором угольной кислоты. После летней грозы в дождевой воде оказывается еще и азотная кислота. Извержения вулканов и сгорание топлива способствуют появлению в дождевой и снеговой воде серной кислоты.
Кислоты в природе • Кислоты постоянно присутствуют вокруг нас. Например, дождевая вода на первый взгляд кажется чистой. На самом деле в ней присутствует немало других веществ. За счет растворения углекислого газа из атмосферы она является раствором угольной кислоты. После летней грозы в дождевой воде оказывается еще и азотная кислота. Извержения вулканов и сгорание топлива способствуют появлению в дождевой и снеговой воде серной кислоты.
 Кислоты в организме человека • Аскорбиновая, фолиевая, оротовая, пангамовая, никотиновая и другие кислоты являются витаминами. • Аминокислоты, соединяясь друг с другом в самых причудливых сочетаниях, образуют великое множество белков. А из них, в свою очередь, строятся почти все ткани нашего организма. • Фосфорная кислота в виде своих кальциевых, магниевых и стронциевых солей – основной «конструкционный материал» костей, зубов, ногтей.
Кислоты в организме человека • Аскорбиновая, фолиевая, оротовая, пангамовая, никотиновая и другие кислоты являются витаминами. • Аминокислоты, соединяясь друг с другом в самых причудливых сочетаниях, образуют великое множество белков. А из них, в свою очередь, строятся почти все ткани нашего организма. • Фосфорная кислота в виде своих кальциевых, магниевых и стронциевых солей – основной «конструкционный материал» костей, зубов, ногтей.
 Кислоты нашей пище • Немало кислот в нашей пище. Фрукты, овощи, молочные продукты, лекарства поставляют целый букет кислот: яблочную, щавелевую, лимонную, миндальную, молочную, масляную, кофейную, уксусную, аскорбиновую и другие. Даже синильная кислота (сильнейший яд) знакома каждому, кто лакомился ядрышками косточек слив, вишен или миндаля. Количество ее мизерно, но ощутить вкус и запах можно. Так что ядрышками увлекаться не следует, особенно если они взяты из недозрелых плодов или
Кислоты нашей пище • Немало кислот в нашей пище. Фрукты, овощи, молочные продукты, лекарства поставляют целый букет кислот: яблочную, щавелевую, лимонную, миндальную, молочную, масляную, кофейную, уксусную, аскорбиновую и другие. Даже синильная кислота (сильнейший яд) знакома каждому, кто лакомился ядрышками косточек слив, вишен или миндаля. Количество ее мизерно, но ощутить вкус и запах можно. Так что ядрышками увлекаться не следует, особенно если они взяты из недозрелых плодов или
 Кислоты в животном мире • Если вы присядете вблизи муравейника, то надолго запомните жгучие укусы его обитателей. Муравей впрыскивает в ранку от укусу яд, содержащий муравьиную кислоту. Муравьиной кислотой обусловлено жжение крапивы, ее выделяют некоторые гусеницы. • Тропический паук стреляет во врагов струйкой жидкости, содержащей 84% уксусной кислоты. • Плоские тысяченожки используют пары синильной кислоты. • Некоторые жуки выстреливают струйкой разбавленной серной кислоты.
Кислоты в животном мире • Если вы присядете вблизи муравейника, то надолго запомните жгучие укусы его обитателей. Муравей впрыскивает в ранку от укусу яд, содержащий муравьиную кислоту. Муравьиной кислотой обусловлено жжение крапивы, ее выделяют некоторые гусеницы. • Тропический паук стреляет во врагов струйкой жидкости, содержащей 84% уксусной кислоты. • Плоские тысяченожки используют пары синильной кислоты. • Некоторые жуки выстреливают струйкой разбавленной серной кислоты.
 Кислоты в растительном мире • • • Многие растения содержат кислоты и используют их как «Химическое оружие» Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито, что мухомору незачем прятаться. Однако лоси жуют мухоморы и не погибают от этого. Скорее – наоборот: мухоморами они лечат какие-то свои «хвори» . Ботаникам известно более 800 видов растений, вырабатывающих синильную кислоту. Многие растения выделяют кислоты, угнетая ими другие виды растений. В волосках крапивы содержится жгучая муравьиная кислота
Кислоты в растительном мире • • • Многие растения содержат кислоты и используют их как «Химическое оружие» Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито, что мухомору незачем прятаться. Однако лоси жуют мухоморы и не погибают от этого. Скорее – наоборот: мухоморами они лечат какие-то свои «хвори» . Ботаникам известно более 800 видов растений, вырабатывающих синильную кислоту. Многие растения выделяют кислоты, угнетая ими другие виды растений. В волосках крапивы содержится жгучая муравьиная кислота
 Роль кислот в создании почвы • Самая значительная функция кислот в природе состоит в разрушении горных пород и создании почвы. Ведь было время, когда вся земная суша представляла собой голые камни. Сотни миллионов лет потребовалось на то, чтобы солнце, ветер и слабый раствор кислот – дождевая вода – разрушили камни на песчинки. Появившиеся затем растения тут же подключились к процессу разрушения горных пород и созданию почвы.
Роль кислот в создании почвы • Самая значительная функция кислот в природе состоит в разрушении горных пород и создании почвы. Ведь было время, когда вся земная суша представляла собой голые камни. Сотни миллионов лет потребовалось на то, чтобы солнце, ветер и слабый раствор кислот – дождевая вода – разрушили камни на песчинки. Появившиеся затем растения тут же подключились к процессу разрушения горных пород и созданию почвы.
present5.com
Урок 4. Сложные вещества – HIMI4KA
В уроке 4 «Сложные вещества» из курса «Химия для чайников» дадим определение химическим соединениям, рассмотрим различия органических и неорганических соединений, а также выясним, что означает качественный и количественный состав. Напоминаю, что в прошлом уроке «Молекулы и простые вещества» мы рассмотрели, что такое молекулы, простые вещества, а также металлы и неметаллы.

Химические элементы существуют не только в виде свободных атомов и простых веществ. Они также могут входить в состав самых различных химических соединений.
Вещества, состоящие из атомов разных химических элементов, называются сложными веществами или химическими соединениями.
Органические и неорганические вещества
Подавляющее большинство химических веществ — это сложные вещества. Вы уже знаете некоторые из них. Вода, метан, сахар, поваренная соль — сложные вещества. Сложные вещества делятся на две группы — неорганические и органические.
Органические вещества
Все органические вещества объединяет главный признак: в их состав обязательно входят атомы углерода. Кроме углерода, в состав органических веществ чаще всего входят атомы водорода, кислорода, а также азота, фосфора, серы. Почти все органические вещества горючи и легко разлагаются при нагревании. Практически все они имеют молекулярное строение (рис. 41).

Простейшим органическим веществом является природный газ метан. Но вам, наверное, знакомы и такие органические вещества, как сахар (сахароза), уксусная и лимонная кислоты, спирт, крахмал, белки, жиры, пластмассы и т. д. Органических веществ миллионы. Они содержатся во всех животных и растительных организмах (откуда и произошло их название), входят в состав пищи, топлива, лекарств, красителей, самых разнообразных материалов.
Неорганические вещества
Неорганические вещества являются соединениями всех остальных элементов. К неорганическим традиционно относят также несколько веществ, содержащих углерод: углекислый и угарный газы, мел, соду и некоторые другие. Неорганических веществ около 700 тыс., но их общая масса многократно превышает массу органических веществ. Почти все они — твердые вещества немолекулярного строения (рис. 42), входят в состав минералов, почв, горных пород.
Качественный и количественный состав веществ
Каждое вещество характеризуется определенным качественным и количественным составом.
Качественный состав вещества показывает, из атомов каких элементов оно состоит. Например, вода состоит из атомов водорода и кислорода, а метан— из атомов углерода и водорода. Число атомов каждого элемента в составе мельчайшей частицы вещества характеризует его количественный состав. Например, молекула воды состоит из двух атомов водорода и одного атома кислорода, а молекула метана — из одного атома углерода и четырех атомов водорода.
Сложное вещество можно с помощью различных химических методов разложить на несколько новых веществ, и так до тех пор, пока не получатся вещества, каждое из которых будет являться простым. Например, сахар при нагревании разлагается на воду и уголь (углерод):
а воду можно разложить с помощью электрического тока на водород и кислород:
Свойства простых веществ, которые при этом получаются (углерода, кислорода и водорода), совершенно не похожи на свойства сложных веществ — сахара и воды. Это разные вещества с разными свойствами. Свойства сложного вещества не являются суммой свойств простых веществ, которые образуются при его разложении.
Сложные вещества, как и простые, имеют либо молекулярное, либо немолекулярное строение. При этом вещества молекулярного строения могут существовать при обычных условиях в различных агрегатных состояниях. Например, метан — газ, вода — жидкость, сахар — твердое вещество.
Вещества немолекулярного строения при обычных условиях — твердые кристаллы, например поваренная соль, мел. Конечно, при нагревании (иногда до нескольких тысяч градусов) такие вещества плавятся, а затем переходят и в парообразное состояние.
Отличия между сложными веществами и смесями веществ
Необходимо различать сложные вещества и смеси веществ:
| Сложное вещество (химическое соединение) | Смесь веществ |
| Образуется в результате соединения атомов различных элементов между собой (химический процесс) | Образуется в результате смешивания различных веществ (физический процесс) |
| Свойства сложного вещества отличаются от свойств простых веществ, из которых оно получено | Свойства веществ, из которых составлена смесь, не изменяются |
| Имеет определенный качественный и количественный состав | Состав произвольный |
| Разлагается на составные части только в результате химических процессов | Разделяется на составные части с помощью различных физических методов |
Краткие выводы урока:
- Сложными называются вещества, состоящие из атомов разных химических элементов.
- Каждое чистое вещество имеет определенный качественный и количественный состав.
- Свойства сложного вещества отличаются от свойств простых веществ, из которых оно получено.
- Сложные вещества имеют молекулярное или немолекулярное строение.
- Все сложные вещества делятся на органические и неорганические.
Надеюсь урок 4 «Сложные вещества» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Вещество в химии - это что? Свойства веществ. Классы веществ
Основной вопрос, на который должен знать ответ человек для правильного понимания картины мира – что такое вещество в химии. Данное понятие формируется ещё в школьном возрасте и направляет ребёнка в дальнейшем развитии. Приступая к изучению химии важно найти точки соприкосновения с ней на бытовом уровне, это позволяет наглядно и доступно разъяснить те или иные процессы, определения, свойства и т.д.
К сожалению, в силу неидеальности системы образования, многие упускают некоторые фундаментальные азы. Понятие «вещество в химии» – это своего рода краеугольный камень, своевременное усвоение данного определения даёт человеку правильный старт в последующем развитии в области естествознания.
Формирование понятия
Перед тем как перейти к понятию вещества, необходимо определить, чем является предмет химии. Вещества – это то, что непосредственно изучает химия, их взаимные превращения, строение и свойства. В общем понимании вещество – это то, из чего состоят физические тела.
Итак, что такое вещество в химии? Сформируем определение путём перехода от общего понятия к чисто химическому. Вещество – это определённый тип материи, обязательно имеющий массу, которую можно измерить. Данная характеристика отличает вещество от другого вида материи – поля, которое массы не имеет (электрическое, магнитное, биополе и т.д.). Материя, в свою очередь, – это то, из чего созданы мы и всё, что нас окружает.
Несколько другая характеристика материи, определяющая то, из чего конкретно она состоит – это уже предмет химии. Вещества сформированы атомами и молекулами (некоторые ионами), а значит любая субстанция, состоящая из этих формульных единиц, и есть вещество.
Простые и сложные вещества
После усвоения базового определения можно перейти к его усложнению. Вещества бывают различных уровней организации, то есть простые и сложные (или соединения) – это самое первое деление на классы веществ, химия имеет множество последующих разделений, подробных и более сложных. Эта классификация, в отличие от многих других, имеет строго определённые границы, каждое соединение можно чётко отнести к одному из видов, взаимоисключающих друг друга.
Простое вещество в химии – это соединение, состоящее из атомов только одного элемента из периодической таблицы Менделеева. Как правило, это бинарные молекулы, то есть состоящие из двух частиц, соединённых посредством ковалентной неполярной связи – образования общей неподелённой электронной пары. Так, атомы одного и того же химического элемента имеют идентичную электроотрицательность, то есть способность удерживать общую электронную плотность, поэтому она не смещена ни к одному из участников связи. Примеры простых веществ (неметаллы) - водород и кислород, хлор, йод, фтор, азот, сера и т.д. Из трёх атомов состоит молекула такого вещества, как озон, а из одного – всех благородных газов (аргона, ксенона, гелия и т.д.). В металлах (магнии, кальции, меди т.д.) существует свой собственный тип связи – металлический, осуществляющийся за счёт обобществления свободных электронов внутри металла, а образования молекул как таковых не наблюдается. При записи вещества металла указывается просто символ химического элемента без каких-либо индексов.
Простое вещество в химии, примеры которого были приведены выше, отличается от сложного качественным составом. Химические соединения образованы атомами разных элементов, от двух и более. В таких веществах имеет место ковалентный полярный или ионный тип связывания. Так как разные атомы имеют отличающуюся электроотрицательность, то при образовании общей электронной пары происходит её сдвиг в сторону более электроотрицательного элемента, что приводит к общей поляризации молекулы. Ионный тип – это крайний случай полярного, когда пара электронов полностью переходит к одному из участников связывания, тогда атомы (или их группы) превращаются в ионы. Чёткой границы, между этими типами нет, ионную связь можно интерпретировать как ковалентную сильно полярную. Примеры сложных веществ - вода, песок, стекло, соли, оксиды и т.д.
Модификации веществ
Вещества, именуемые простыми, на самом деле имеют уникальную особенность, которая не присуща сложным. Некоторые химические элементы могут образовывать несколько форм простого вещества. В основе всё так же лежит один элемент, но количественный состав, строение и свойства кардинально отличают такие образования. Эта особенность имеет название аллотропии.
Кислород, сера, углерод и другие элементы имеют несколько аллотропных модификаций. Для кислорода – это О2 и О3, углерод даёт четыре типа веществ – карбин, алмаз, графит и фуллерены, молекула серы бывает ромбической, моноклинной и пластической модификации. Такое простое вещество в химии, примеры которого не ограничены вышеперечисленными, имеет огромное значение. В частности, фуллерены используются как полупроводники в технике, фоторезисторы, добавки для роста алмазных плёнок и в других целях, а в медицине это мощнейшие антиоксиданты.
Что происходит с веществами?
Каждую секунду внутри и вокруг происходит превращение веществ. Химия рассматривает и объясняет те процессы, которые идут с качественным и/или количественным изменением состава реагирующих молекул. Параллельно, часто взаимосвязано протекают и физические превращения, которые характеризуются лишь изменением формы, цвета веществ или агрегатного состояния и некоторых других характеристик.
Химические явления – это реакции взаимодействия различных видов, например, соединения, замещения, обмена, разложения, обратимые, экзотермические, окислительно-восстановительные и т.д., в зависимости от изменения интересующего параметра. К физическим явлениям относят: испарение, конденсацию, сублимацию, растворение, замерзание, электропроводимость и т.д. Часто они сопровождают друг друга, например, молния во время грозы – это физический процесс, а выделение под её действием озона – химический.
Физические свойства
Вещество в химии – это материя, которой присущи определённые физические свойства. По их наличию, отсутствию, степени и интенсивности можно спрогнозировать, как вещество поведёт себя в тех или иных условиях, а также объяснить некоторые химические особенности соединений. Так, например, высокие температуры кипения органических соединений, в которых есть водород и электроотрицательный гетероатом (азот, кислород и т.д.), свидетельствуют о том, что в веществе проявляется такой химический тип взаимодействия, как водородная связь. Благодаря знанию о том, какие вещества имеют наилучшую способность проводить электрический ток, кабеля и провода электропроводки изготавливаются именно из определённых металлов.
Химические свойства
Установлением, исследованием и изучением другой стороны медали свойств занимается химия. Свойства веществ с её точки зрения – это их реакционная способность к взаимодействию. Некоторые вещества крайне активны в этом смысле, например, металлы или любые окислители, а другие, благородные (инертные) газы, при нормальных условиях в реакции практически не вступают. Химические свойства можно активировать или пассивировать при необходимости, иногда это не связано с особыми трудностями, а в некоторых случаях приходится нелегко. Учёные проводят многие часы в лабораториях, методом проб и ошибок добиваясь поставленных целей, иногда и не достигают их. Изменяя параметры окружающей среды (температуру, давление и т.д.) или применяя специальные соединения – катализаторы или ингибиторы - можно повлиять на химические свойства веществ, а значит и на ход реакции.
Классификация химических веществ
В основе всех классификаций лежит разделение соединений на органические и неорганические. Главный элемент органики – это углерод, соединяясь друг с другом и гидрогеном, атомы карбона образуют углеводородный скелет, который после заполняется другими атомами (кислородом, азотом, фосфором, серой, галогенами, металлами и другими), замыкается в циклы или разветвляется, обосновывая тем самым большое разнообразие органических соединений. На сегодняшний день науке известны 20 миллионов таких веществ. В то время как минеральных соединений всего лишь полмиллиона.
Каждое соединение индивидуально, но имеет и множество похожих черт с другими в свойствах, строении и составе, на этой основе происходит группировка в классы веществ. Химия имеет высокий уровень систематизации и организации, это точная наука.
Неорганические вещества
1. Оксиды – бинарные соединения с кислородом:
а) кислотные – при взаимодействии с водой дают кислоту;
б) основные – при взаимодействии с водой дают основание.
2. Кислоты – вещества, состоящие из одного или нескольких протонов водорода и кислотного остатка.
3. Основания (щёлочи) – состоят из одной или нескольких гидроксильных групп и атома металла:
а) амфотерные гидроксиды – проявляют свойства и кислот и оснований.
4. Соли – результат реакции нейтрализации между кислотой и щелочью (растворимым основанием), состоят из атома металла и одного или нескольких кислотных остатков:
а) кислые соли – анион кислотного остатка имеет в составе протон, результат неполной диссоциации кислоты;
б) основные соли – с металлом связана гидроксильная группа, результат неполной диссоциации основания.
Органические соединения
Классов веществ в органике великое множество, такой объём информации сложно сразу запомнить. Главное, знать основные разделения на алифатические и циклические соединения, карбоциклические и гетероциклические, предельные и непредельные. Также углеводороды имеют множество производных, в которых атом гидрогена замещён на галоген, кислород, азот и другие атомы, а так же функциональные группы.
Вещество в химии - это основа сущестования. Благодаря органическому синтезу человек на сегодняшний день имеет огромное количество искусственных веществ, заменяющих натуральные, а также не имеющих аналогов по своим характеристикам в природе.
fb.ru
Простые и сложные вещества - Первоначальные химические понятия Химия 7 класс Савчин М.М. - Грамота 2015 год
Тема 1 Первоначальные химические понятия
§ 9. Простые и сложные вещества
Освоив эту тему, вы сможете:
• различать понятия «простое вещество» и «сложное вещество», формулы простых и сложных веществ;
• понимать понятие «химическое соединение»;
• приводить примеры простых и сложных веществ;
• описывать простые и сложные вещества, известные вам из повседневного обихода;
• высказывать суждения о многообразии веществ.
Большинство атомов химических элементов обладают способностью сочетаться друг с другом или с атомами других химических элементов. Вследствие этого образуются химические соединения. Независимо от состава их структурных частиц и простые, и сложные вещества являются химическими соединениями, так как между ними возникают химические связи.
Вы уже ознакомились со строением атомов химических элементов. Вещества, составляющими которых являются атомы, называют атомными.
Однако среди всего разнообразия химических соединений существуют и молекулярные вещества. Составной частью их являются молекулы.
Молекулы — мельчайшие частицы вещества, сохраняющие его химические свойства.
Молекулу считают пределом делимости вещества. Если она разрушается, то разрушается и вещество. Характерной особенностью молекул является непрерывное движение.
- Вспомните из курса природоведения, какое явление называется диффузией.
Каждая молекула состоит из определенного количества атомов одного или различных химических элементов.
- Вспомните из курса природоведения, как делятся вещества по составу и происхождению.
Какие вещества называют: а) простыми; б) сложными? Приведите несколько примеров простых и сложных веществ, которыми вы чаще всего пользуетесь в быту.
Простые вещества — это вещества, образованные одним химическим элементом.
Например, простые вещества водород, кислород, азот образованные в соответствии химическими элементами Гідрогеном, Оксигеном, Азотом. В состав их молекул входят по два соединенные между собой атомы этих элементов (рис. 41 а, 6, в).
Элемент Кислород при определенных условиях образует еще одну простую вещество — озон, молекула которого содержит три атома (рис. 41 г).
Рис. 41. Модели молекул простых веществ: а — водорода; б — кислород; в — озона; г — азота
Сложные вещества — это вещества, образованные двумя или более химическими элементами.
К сложным веществам относятся; вода, сахар, мыло, поваренная соль, мел, метан (составляющая природного газа), углекислый газ. Вещества, входящие в состав клеток живых организмов (белки, жиры и углеводы), являются сложными и содержат преимущественно атомы Углерода, Кислорода, Водорода, Азота, Серы, Фосфора и имеют молекулярное строение.
- Вспомните, как доказать, что вода является сложным веществом. Какие методы исследования использовали ученые, чтобы определить состав воды?
На рисунке 42 изображена модели молекул метана, углекислого газа и воды. Молекула метана состоит из одного атома Углерода и четырех атомов Водорода, молекула углекислого газа — из одного атома Карбона и двух атомов Кислорода, молекула воды — из одного атома Кислорода и двух атомов Водорода.
Рис. 42. Модели молекул сложных веществ: а — метана; б — углекислого газа; в — воды
Итак, в зависимости от состава, вещества классифицируют на простые и сложные. Схему классификации веществ изображено на рисунке 43.
Рис. 43. Классификация веществ
Простые вещества: металлы и неметаллы. Простые вещества разделяют па две группы. Металлические элементы образуют металлы, нерудные — неметаллы. Их различают по физическим свойствам.
- Вспомните, с какими физическими свойствами веществ вы уже ознакомились. Назовите их.
Обратимся к демонстрациям и рассмотрим образцы простых веществ металлов и неметаллов. Из металлов наиболее распространенными в технике, различных отраслях производств, быту с железо, цинк, алюминий, медь, серебро, золото; из неметаллов в лаборатории имеются сера, углерод, красный фосфор, бром, йод.
- Обратите внимание на агрегатное состояние металлов и неметаллов. Почему, по вашему мнению, бром хранят в запаянных ампулах?
За основу деления простых веществ па металлы и неметаллы взято их физические свойства (табл. 2).
Таблица 2
Физические свойства простых веществ
| Металлы | Неметаллы |
| Металлический блеск | Не имеют металлического блеска |
| Электропроводящие | Неелектропровідні |
| Теплопроводные | Нетеплопровідні |
| Высокие температуры плавления | Низкие температуры плавления |
| Пластические, ковкі | Хрупкие |
| Нелетучие | Летучие Некоторые из них имеют характерный запах |
Неметаллы — это вещества, которые по большей части состоят из молекул. Молекулы многих из них двухатомные. Однако встречаются и многоатомные молекулы: уже упоминавшийся озон, кристаллическая сера — содержит восемь атомов Серы, белый фосфор — четыре атома этого элемента. В простых веществах, образованных элементом Карбоном, атомы соединяются в определенном порядке, не образуя молекул.
Металлы состоят из атомов соответствующих элементов. Названия металлов часто совпадают с названиями металлических элементов, их образующих. Например, вещества алюминий, цинк, никель, хром, магний образованные соответствующими химическими элементами. Однако вещество медь состоит из атомов элемента Купруму, серебро — Аргентуму, золото — Ауруму, ртуть — Меркурию, железо — Железа. В названия неметаллов элементов и простых веществ совпадают для незначительного количества веществ (табл. 3).
Таблица С
Названия химических элементов и простых веществ
| Металлические | Неметаллические | ||
| Химический элемент | Простое вещество | Химический элемент | Простое вещество |
| Алюминий | алюминий | Арсен | арсен |
| Аргентум | серебро | Бром | бром |
| Аурум | золото | Водород | водород |
| Купрум | медь | Йод | йод |
| Магний | магний | Карбон | углерод |
| Манган | манган | Азот | азот |
| Меркурий | ртуть | Оксиген | кислород |
| Платина | платина | Силиция | силиция |
| Плюмбум | свинец | Сульфур | сера |
| Станум | олово | Фтора | фтор |
| Ферум | железо | Фосфор | фосфор |
| Хром | хром | Хлор | хлор |
Лабораторный опыт 2
Ознакомление с образцами простых и сложных веществ
Задача 1. Рассмотрите внимательно вещества, выданные вам в банках. Прочтите надписи на этикетках: Н2О (вода), S (сера), Р (фосфор), Mg (магний), NaOH (натрия гидроксид), С (углерод), Fe3O4 (ферум(II, III) оксид), Fе (железо), ZnO (цинк оксид), СаСО3 (кальций карбонат), Аl (алюминий), Zn (цинк), СаО (кальций оксид), Nа2СО3 (натрий карбонат).
Распределите эти вещества на две группы: простые и сложные. Простые классифицируйте вещества на металлы и неметаллы.
Задание 2. Опишите: а) чем отличаются по составу простые и сложные вещества; 6) по каким признакам вы сделали классификацию.
Задание 3. Опишите физические свойства веществ на основе ваших наблюдений.
Выполнив задание, запишите данные в рабочую тетрадь в виде таблицы. В конце работы сформулируйте выводы.
| Простые вещества | Описание свойств по наблюдениям | Сложные вещества | Описание свойств по наблюдениям |
| Металлы | |||
| Неметаллы | |||
Многообразие веществ. Многообразие веществ объясняется способностью атомов элементов сочетаться между собой. В зависимости от того, какие атомы, в каком количестве и как соединяются, образуется много простых и сложных веществ (рис. 44).
Рис. 44. Простое вещество сера (а) и сложное вещество аметист (б)
Простых веществ существует чуть больше, чем химических элементов — 400, ибо, как вы уже знаете, один и тот же элемент (Оксиген, Карбон, Фосфор, Сульфур) может образовывать две или более веществ.
Сложных веществ известно гораздо больше (почти 20 милл). Это вода, в состав молекулы которого входят Водород и Кислород, углекислый газ — Карбон и Кислород, поваренная соль — Натрий и Хлор. В состав названных веществ входят только два элемента — это бинарные соединения. Однако значительное количество веществ состоит из трех и более элементов. Так, в состав глюкозы входят три элемента: Карбон, Гидроген и Оксиген, а питьевая сода содержит четыре элемента: Натрий, Водород, Карбон и Кислород.
К сложным относятся все органические вещества. Кроме того, существует целая индустрия по добыче синтетических и искусственных соединений, которые имеют огромное производственное и бытовое назначение.
- Вспомните из курса природоведения, какие вещества называют неорганическими, органическими. Приведите примеры неорганических и органических соединений.
При нормальных условиях (температура 0 °С, давление 101,3 кПа) вещества находятся в трех агрегатных состояниях: жидком (вода, масло, спирт), твердом (цинк, железо, сера, фосфор, углерод, медь) и газуватому (водород, кислород, озон, азот, углекислый газ, инертные газы).
СУММИРУЕМ ИЗУЧЕННОЕ
• Вещества подразделяют на простые и сложные.
• Сложные вещества образуются из двух и более химических элементов. их значительно больше, чем простых.
• Каждая простое и сложное вещество характеризуется определенными свойствами, то есть признаками, по которым можно выявить их сходство и различие.
• Сложные вещества бывают органического и неорганического происхождения.
• Многообразие веществ объясняется способностью атомов элементов сочетаться между собой.
ЗАДАНИЯ ДЛЯ КОНТРОЛЯ ЗНАНИЙ
1. Объясните, что означают понятия «молекула», «простое вещество», «сложное вещество», «химическое соединение».
2. Приведите примеры: а) простых и сложных веществах; б) органических и неорганических веществ.
3. Обоснуйте, являются ли идентичными понятия «химическое соединение» и «смесь веществ».
4. Охарактеризуйте физические свойства: а) сахара; б) воды; в) масла.
5. Обоснуйте, почему сложных веществ больше, чем простых.
6. Выскажите собственное суждение о важности веществ для жизни и здоровья человека.
ИНТЕРЕСНО ЗНАТЬ
Английский химик Г. Дэви впервые выделил в свободном состоянии, методом электролиза, металлы натрий, калий, кальций, стронций, барий, магний. Эти работы положили начало изготовления сильных ламп для прожекторов, маяков и т. др. Впоследствии ученый создал безопасную шахтерскую лампу, которая использовалась во всем мире, пока не была заменена лампочкой с аккумулятором.
Склодовская-Кюри Мария (1867-1934) — французский физик и химик, педагог, общественный деятель. Наука обязана ему открытием и исследованием двух радиоактивных элементов — Полония и Радия. Открытие элемента Радия начало метод лечение им рака кожи. За свой труд была награждена двумя Нобелевскими премиями, которые пожертвовала на строительство санатория в г. Закопане и Радиологического института в г. Варшаве (Польша).
schooled.ru
Простые вещества - это... Что такое Простые вещества?
Простые вещества — вещества, состоящие исключительно из атомов одного химического элемента (из гомоядерных молекул)[1][2], в отличие от сложных веществ. Являются формой существования химических элементов в свободном виде[1][3]; или, иначе говоря, элементы, не связанные химически ни с каким другим элементом, образуют простые вещества[3]. Известно свыше 400 разновидностей простых веществ[2].
В зависимости от типа химической связи между атомами простые вещества могут быть металлами (Na, Mg, Al, Bi и др.) и неметаллами (h3, N2, Br2, Si и др.)[2].
Примеры простых веществ: молекулярные (O2, O3, h3, Cl2) и атомарные (He, Ar) газы; различные формы углерода, иод (I2), металлы (не в виде сплавов).
Аллотропные модификации
Схемы строения различных модификаций углеродаa: алмаз, b: графит, c: лонсдейлитd: фуллерен — букибол C60, e: фуллерен C540, f: фуллерен C70g: аморфный углерод, h: углеродная нанотрубкаОдин и тот же химический элемент зачастую может образовывать несколько типов простых веществ (аллотропия), называемых аллотропными модификациями. Явление аллотропии может быть обусловлено либо различным составом молекул данного элемента (аллотропия состава), либо различным строением молекул и способом размещения молекул (атомов) в кристаллах (аллотропия формы). Способность элемента к образованию соответствующих аллотропных модификаций обусловлена строением атома, которое определяет тип химической связи, строение молекул и кристаллов[2].
Различные аллотропные модификации могут переходить друг в друга. Для данного химического элемента его аллотропные модификации всегда различаются по физическим свойствам и химической активности (например, озон активнее кислорода, температура плавления алмаза больше, чем фуллерена)[4].
При нормальных условиях соответствующие простые вещества для 11 элементов являются газами (H, He, N, O, F, Ne, Cl, Ar, Kr, Xe, Rn), для 2 — жидкостями (Br, Hg), для остальных элементов — твёрдыми телами.
При комнатной температуре (либо близкой к ней) 5 металлов находятся в жидком либо полужидком состоянии, так как их температура плавления близка к комнатной:
Отношение понятий
Понятия «атом», «химический элемент» и «простое вещество» не следует смешивать. «Атом» — конкретное понятие, так как атомы существуют реально. «Химический элемент» — это собирательное, абстрактное понятие; в природе химический элемент существует в виде свободных или химически связанных атомов, то есть простых и сложных веществ.
Также нужно различать свойства (характеристики) простого вещества (совокупности частиц) и свойства (характеристики) химического элемента (изолированного атома определенного вида), см. таблицу ниже[4]:
Названия химических элементов и соответствующих простых веществ совпадают в большинстве случаев. Однако существуют и исключения. Например, названия аллотропных модификаций кислорода — кислород (дикислород O2) и озон; углерода — алмаз, графит, карбин, фуллерен.
Каждый химический элемент имеет свое условное обозначение — химический знак (символ). В ряде случаев химический знак может также выражать состав простого вещества (Zn, B, C, Ar). Однако, например, символ O обозначает только химический элемент, простое вещество «кислород» имеет формулу O2.
См. также
Примечания
- ↑ 1 2 Редкол.:Кнунянц И. Л. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1988. — Т. 1. — С. 361. — 623 с. — 100 000 экз.
- ↑ 1 2 3 4 Ахметов Н.С. Общая и неорганическая химия. — 4 изд., испр. — Москва: Высшая школа, Издательский центр «Академия», 2001. — С. 253-269. — 743 с. — 15 000 экз. — ISBN 5-06-003363-5, 5-7695-0704-7
- ↑ 1 2 Глинка Н.Л. Общая химия. — 24 изд., испр. — Ленинград: Химия, 1985. — С. 18-19. — 702 с.
- ↑ 1 2 Врублевский А.И. Химия: базовый школьный курс. — Минск: Юнипресс, 2009. — С. 11-12. — 576 с. — 3 100 экз. — ISBN 978-985-507-813-6
Литература
- Ахметов Н.С. Общая и неорганическая химия. — 4 изд., испр. — Москва: Высшая школа, Издательский центр «Академия», 2001. — 743 с. — 15 000 экз. — ISBN 5-06-003363-5, 5-7695-0704-7.
- Врублевский А.И. Химия: базовый школьный курс. — Минск: Юнипресс, 2009. — 576 с. — 3 100 экз. — ISBN 978-985-507-813-6.
Ссылки
dic.academic.ru











