Содержание
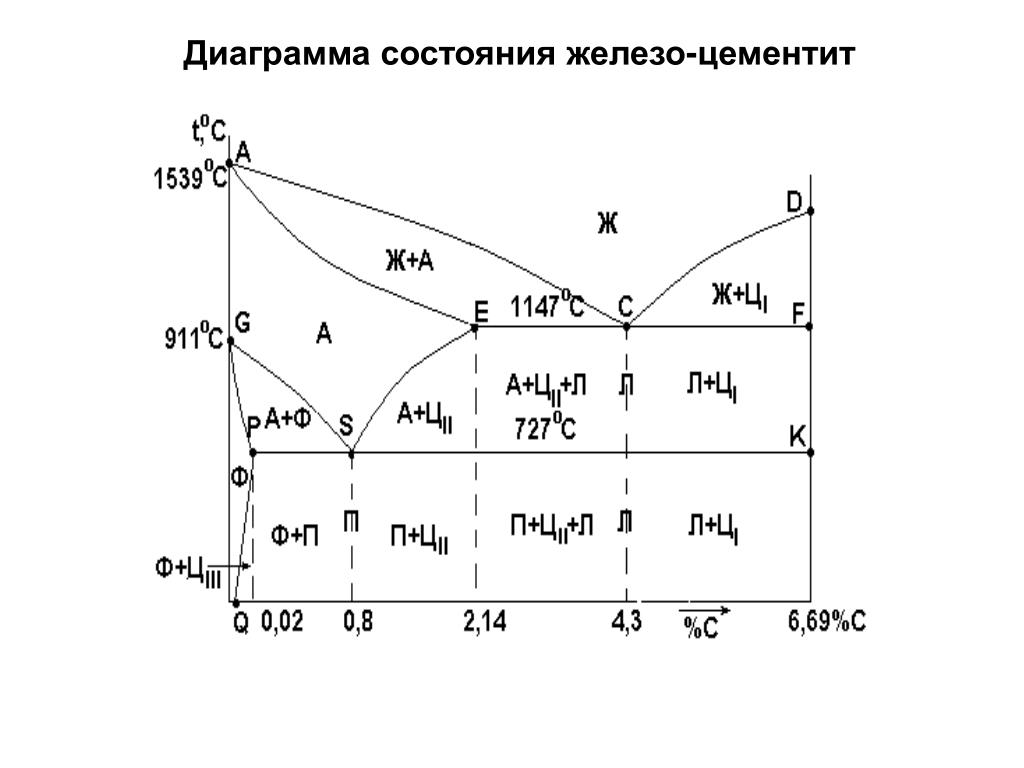
Диаграмма состояния «железо — углерод»
Диаграмма состояния железо-углерод (цементит) — это графическое отображение фазового состава и структуры сплавов в зависимости от концентрации углерода и температуры
Содержание
- Компоненты в системе «железо-углерод»
- Железо
- Углерод
- Цементит
- Фазы в системе «железо-углерод»
- Жидкая фаза
- Феррит
- Аустенит в сталях
- Цементит – формы существования
- Другие структурные составляющие в системе «железо-углерод»
- Перлит
- Ледебурит в сталях
- Узловые критические точки диаграммы состояния системы железо-углерод
- Значение линий диаграммы состояния системы железо-углерод
Компоненты в системе «железо-углерод»
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит:
Железо
Железо – d-переходный металл серебристо-светлого цвета. Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3. Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
Температура плавления – 1539° С. Удельный вес равен 7,86 г/см3. Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях — α и γ. Полиморфные превращения происходят при температурах 911° С и 1392° С. При температуре ниже 911° С и выше 1392° С существует Feα (или α-Fе) с объемно-центрированной кубической решеткой. В интервале температур 911…1392° С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539° С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
При температуре ниже 768° С железо ферромагнитно, а выше – парамагнитно. Точку 768° С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное называют точкой Кюри. Модификация Feγ парамагнитна.
Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (временное сопротивление – σв=250 МПа, предел текучести – σт=120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ=50 %, а относительное сужение – ψ=80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод
Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500° С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000° С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260° С. Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210° С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: например, азотом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
Фазы в системе «железо-углерод»
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Жидкая фаза
Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
Феррит
Феррит (Ф, α)- твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727° С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539° С) с предельной растворимостью углерода 0,1 % при температуре 1499° С (точка J).
Свойства феррита близки к свойствам железа. Он мягок (твердость – 80 — 130 НВ, временное сопротивление – σв=300 МПа) и пластичен (относительное удлинение — δ=50 %), магнитен до 768° С.
Под микроскопом феррит выглядит как светлые полиэдрические зерна. В сталях может существовать в виде сетки (разной толщины, в зависимости от содержания углерода), зерен (малоуглеродистые стали), пластин или игл (видманштетт).
Аустенит в сталях
Аустенит (А, γ) – твердый раствор внедрения углерода в γ–железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Предельная растворимость углерода в γ -железе 2,14 % при температуре 1147° С (точка Е). Аустенит имеет твердость 180 НВ, пластичен (относительное удлинение – δ=40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования. Под микроскопом выглядит как светлые полиэдрические зерна с двойниками.
Цементит – формы существования
В железоуглеродистых сплавах присутствуют фазы: цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо — цементит и железо — графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе — С) — графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат: температура — содержание углерода. Диаграмма состояния системы железо — углерод построена по результатам многочисленных исследований, проведенных учеными ряда стран. Особое место среди них занимают работы Д.К. Чернова. Он открыл существование критических точек в стали, определил их зависимость от содержания углерода, заложил основы для построения диаграммы состояния железоуглеродистых сплавов в ее нижней, наиболее важной части.
Буквенное обозначение узловых точек в диаграмме является общепринятым как в России, так и за рубежом.
Диаграмма состояния железо-углерод
Имеющиеся во всех областях диаграммы фазы видны на рисунке. Значение всех линий указано в таблице.
Значение всех линий указано в таблице.
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус — по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % — к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения. Обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии GS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) — как Аr1.
Другие структурные составляющие в системе «железо-углерод»
Кроме компонентов и фаз в системе сплавов «железо-углерод» присутствуют другие структурные составляющие — перлит и ледебурит
Перлит
Перлит — эвтектоид, механическая смесь феррита и цементита, полученная в результате распада аустенита при охлаждении сплавов ниже 727° С. При медленном охлаждении перлит присутствует во всех сплавах с концентрацией углерода от 0,02 до 6,67%. Под микроскопом перлит может выглядеть либо как пластины, либо как зерна — зернистый перлит. Его вид, также как и механические свойства, зависит от скорости охлаждения сплава и вида его термической обработки
Ледебурит в сталях
Ледебурит — эвтектика, механическая смесь аустенита и цементита, выделяющаяся из жидкости при охлаждении сплавов ниже 1147° С. Принципиальное отличие эвтектикой составляющей от эвтектоидной заключается в том, что первая выделяется из жидкости, а вторая из твердого раствора, в случае железоуглеродистых сплавов — из аустенита. Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Название данная структурная составляющая получила в честь имени немецкого ученого-металлурга Ледебура.
Узловые критические точки диаграммы состояния системы железо-углерод
Узловые критические точки диаграммы железо-углерод
Значение линий диаграммы состояния системы железо-углерод
Значения линий на диаграмме железо-углерод
Всякая диаграмма состояния показывает условия равновесного сосуществования фаз во взятой системе компонентов.
Полное физико-химическое равновесие между фазами может быть достигнуто только в специальных лабораторных условиях, а на практике некоторым приближением к этому состоянию может быть случай чрезвычайно медленного охлаждения или нагрева сплава с весьма длительными выдержками во времени при любых искомых температурах.
Строение сплавов стали
Сплавы — сложные металлические тела, полученные из двух и более элементов (компонентов). Свойства сплава резко отличаются от свойств исходных компонентов. Даже незначительные добавки одного компонента к другому изменяют свойства первоначального взятого вещества.
Даже незначительные добавки одного компонента к другому изменяют свойства первоначального взятого вещества.
У сплавов есть большое сродство с растворами. Как и водные жидкие растворы (сахара, соли и др.) металлические твердые растворы могут иметь различную концентрацию.
Большое влияние на растворимость оказывает температура. С повышением температуры растворимость увеличивается. В металле при понижении температуры происходят почти такие же процессы, как и при обычном растворении соли в воде. В горячей воде можно растворить большее количество соли, чем в холодной. Если охладить насыщенный солью раствор, не имеющий осадка, в нем начнут выпадать кристаллы соли. Если опять нагреть раствор, соль растворится.
Твердый раствор в металле аналогичен охлаждаемому раствору соли в воде в тот момент, когда начинают выпадать кристаллы. Но есть между этими растворами и существенные различия. В жидком растворе атомы растворенного вещества находятся в непрерывном и беспорядочном движении. В твердом растворе атомы растворенного вещества занимают определенное пространственное положение, в зависимости от строения кристаллической решетки.
В твердом растворе атомы растворенного вещества занимают определенное пространственное положение, в зависимости от строения кристаллической решетки.
Различают два основных вида твердых растворов: твердые растворы замещения и твердые растворы внедрения. В нервом атомы растворенного вещества занимают в кристаллической решетке места атомов растворителя, во втором — они внедрены в пространстве между атомами растворителя. Твердые растворы состоят из однородных по составу и строению кристаллов.
При затвердевании большинство сплавов образуют смеси из кристаллов, различающихся по строению и составу (сплавы меди и висмута, свинца и сурьмы и др.). При строго определенной концентрации сплав может представлять собой химическое соединение двух или более компонентов. В отличие от чистых металлов и твердых растворов химические соединения имеют сложную кристаллическую решетку, не похожую на кристаллические решетки исходных компонентов.
В сложных твердых сплавах, состоящих из нескольких компонентов, могут одновременно существовать твердые растворы, смеси различных чистых компонентов и химические соединения. При переходе из жидкого состояния в твердое сплавы испытывают превращения, сопровождающиеся изменением их внутреннего строения (структуры и свойств). Эти структурные превращения для сплавов конкретных составов происходят при определенных температурах.
При переходе из жидкого состояния в твердое сплавы испытывают превращения, сопровождающиеся изменением их внутреннего строения (структуры и свойств). Эти структурные превращения для сплавов конкретных составов происходят при определенных температурах.
Температуры, при которых начинается или заканчивается структурное превращение в сплаве, называются критическими. При критических температурах атомы сплава перестраиваются и образуют новую кристаллическую решетку. Вновь образовавшаяся разновидность сплава по структуре отличается от предшествующего состояния этого же сплава.
В сплаве могут быть две и более структурные разновидности, отделенные одна от другой поверхностями раздела. Однородная часть сплава, отделенная от остальных частей поверхностью раздела, называется фазой. Изменения в структуре сплава при изменении температуры называются структурными, или фазовыми превращениями.
Чистый металл при обычной температуре является однофазным твердым веществом. В расплавленном состоянии чистый металл также является однофазным жидким веществом. Однако при переходе из жидкого в твердое состояние чистый металл имеет одновременно две фазы: жидкую и твердую.
Однако при переходе из жидкого в твердое состояние чистый металл имеет одновременно две фазы: жидкую и твердую.
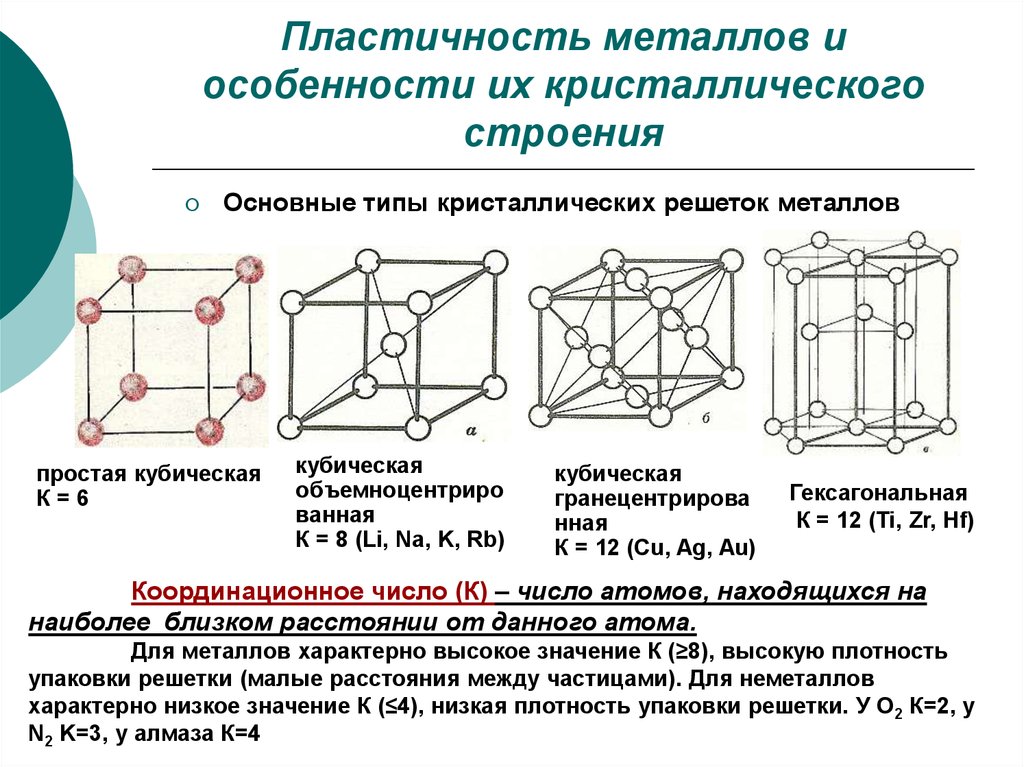
Железо в твердом состоянии может быть двухфазным и иметь две различные кристаллические решетки: a-Fe (альфа-железо) — при температуре ниже 910° С и y-Fe (гамма-железо) — при температуре выше 910° С. Кристаллическая решетка a-Fe — объемно-центрированный куб, Y-Fe — гранецентрированный куб.
Область существования каждой решетки железа можно определить при охлаждении железа от температуры плавления до нормальной. Температура 910° С является критической для превращения одного вида решетки в другой.
В отличие от чистых металлов в сплавах наблюдается большое количество превращений. В сплавах железа с углеродом (углеродистых сталях) железо и углерод взаимодействуют, образуя различные твердые растворы, химические соединения и смеси.
Твердый раствор углерода и примесей (кремния, марганца, серы, фосфора) в a-Fe называется ферритом. От чистого железа феррит отличается только тем, что в его кристаллической решетке, кроме атомов железа, есть небольшое количество атомов углерода и примесей.
Растворимость углерода в железе неодинакова при различных температурах. При температуре 1130° С в железе может раствориться —2% углерода, при 723° С — не более 0,8% углерода. С понижением температуры углерод выделяется из раствора и может соединяться с другими компонентами сплава. Кроме того, углерод может соединяться с железом, образуя химическое соединение.
Химические соединение железа с углеродом называется цементитом (карбид железа), смесь феррита с цементитом — перлитом.
Таким образом, в сплавах железа с углеродом (в углеродистых сталях) железо, углерод и примеси могут образовывать твердые растворы (феррит, аустенит) химическое соединение (цементит) и смесь (перлит). В легированных нержавеющий сталях образуются химические соединения легирующих элементов с углеродом, которые называются карбидами (карбид хрома, карбид титана и др.). Кроме того, в нержавеющих легированных сталях образуются химические соединения железа и легирующих элементов с азотом, которые называются нитридами.
материалов —
материалов —
| ||||||||||||||||
Материалы | ||||||||||||||||
Межстраничное объявление | ||||||||||||||||
Низкоуглеродистый | ||||||||||||||||
От кого: | ||||||||||||||||
10.5: Твердое состояние материи
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 38214
- OpenStax
- OpenStax
Цели обучения
- Дать определение и описать связь и свойства ионных, молекулярных, металлических и ковалентно-сетчатых кристаллических твердых тел
- Описать основные типы кристаллических твердых тел: ионные твердые тела, металлические твердые тела, твердые тела с ковалентной сеткой и молекулярные твердые тела
- Объясните, каким образом кристаллические дефекты могут возникать в твердом
Когда большинство жидкостей охлаждаются, они в конечном итоге замерзают и образуют кристаллические твердые тела, в которых атомы, ионы или молекулы располагаются в определенном повторяющемся порядке. Жидкость также может замерзнуть до того, как ее молекулы выстроятся в упорядоченную структуру. Полученные материалы называются аморфными твердыми телами или некристаллическими твердыми телами (или иногда стеклами). Частицы таких твердых тел лишены упорядоченной внутренней структуры и расположены беспорядочно (рис. \(\PageIndex{1}\)).
Жидкость также может замерзнуть до того, как ее молекулы выстроятся в упорядоченную структуру. Полученные материалы называются аморфными твердыми телами или некристаллическими твердыми телами (или иногда стеклами). Частицы таких твердых тел лишены упорядоченной внутренней структуры и расположены беспорядочно (рис. \(\PageIndex{1}\)).
Рисунок \(\PageIndex{1}\): Объекты твердой фазы могут быть расположены регулярно, повторяющимся образом (кристаллические твердые тела) или случайным образом (аморфно). Кристаллическое расположение представляет собой множество кругов, нарисованных рядами и плотно сложенных друг с другом. Аморфное расположение показывает множество кругов, слегка раздвинутых друг от друга и не образующих организованного узора.
Металлы и ионные соединения обычно образуют упорядоченные кристаллические тела. Вещества, состоящие из больших молекул или смеси молекул, движения которых более ограничены, часто образуют аморфные твердые тела. Например, свечной воск представляет собой аморфные твердые вещества, состоящие из больших молекул углеводородов. Некоторые вещества, такие как оксид бора (рис. \(\PageIndex{2}\)), могут образовывать кристаллические или аморфные твердые тела в зависимости от условий, в которых они производятся. Кроме того, аморфные твердые тела могут переходить в кристаллическое состояние при соответствующих условиях.
Некоторые вещества, такие как оксид бора (рис. \(\PageIndex{2}\)), могут образовывать кристаллические или аморфные твердые тела в зависимости от условий, в которых они производятся. Кроме того, аморфные твердые тела могут переходить в кристаллическое состояние при соответствующих условиях.
Рисунок \(\PageIndex{2}\): (a) Триоксид дибора, B 2 O 3 , обычно встречается в виде белого аморфного твердого вещества (стекло), которое имеет высокую степень беспорядка в своей структуре. . (b) При осторожном длительном нагревании его можно превратить в кристаллическую форму B 2 O 3 , , которая имеет очень упорядоченное расположение. Первая структура триоксида дибора показывает пять идентичных и разделенных гексагональных колец. Вторая структура триоксида дибора представляет собой более взаимосвязанную структуру с четырьмя большими кольцами, образующими более стабильную структуру.
Кристаллические твердые тела обычно классифицируют в соответствии с природой сил, удерживающих их частицы вместе. Эти силы в первую очередь ответственны за физические свойства сыпучих материалов. В следующих разделах дается описание основных типов кристаллических твердых тел: ионных, металлических, ковалентно-сетчатых и молекулярных.
Эти силы в первую очередь ответственны за физические свойства сыпучих материалов. В следующих разделах дается описание основных типов кристаллических твердых тел: ионных, металлических, ковалентно-сетчатых и молекулярных.
Ионные твердые вещества
Ионные твердые вещества, такие как хлорид натрия и оксид никеля, состоят из положительных и отрицательных ионов, удерживаемых вместе за счет электростатического притяжения, которое может быть довольно сильным (рис. \(\PageIndex{3}\)). Многие ионные кристаллы также имеют высокие температуры плавления. Это происходит из-за очень сильного притяжения между ионами — в ионных соединениях притяжение между полными зарядами (намного) больше, чем между частичными зарядами в полярных молекулярных соединениях. Это будет рассмотрено более подробно при более позднем обсуждении энергий решетки. Хотя они твердые, они также имеют тенденцию быть хрупкими и скорее ломаются, чем гнутся. Ионные твердые вещества не проводят электричество; однако они проводят в расплавленном или растворенном состоянии, потому что их ионы могут свободно двигаться. Многие простые соединения, образованные реакцией металлического элемента с неметаллическим элементом, являются ионными.
Многие простые соединения, образованные реакцией металлического элемента с неметаллическим элементом, являются ионными.
Рисунок \(\PageIndex{3}\): Хлорид натрия представляет собой ионное твердое вещество. Показан куб, состоящий из фиолетовых и зеленых сфер. Куб имеет размеры три на три сферы. Фиолетовые сферы немного больше зеленых сфер.
Металлические твердые тела
Металлические твердые тела, такие как кристаллы меди, алюминия и железа, образованы атомами металла. Рисунок \(\PageIndex{4}\). Структуру металлических кристаллов часто описывают как равномерное распределение атомных ядер в «море» делокализованных электронов. Атомы внутри такого твердого металла удерживаются вместе уникальной силой, известной как металлическая связь , которая обеспечивает множество полезных и разнообразных объемных свойств. Все они обладают высокой тепло- и электропроводностью, металлическим блеском и пластичностью. Многие очень жесткие и достаточно сильные. Из-за своей пластичности (способность деформироваться под давлением или ударом молотка) они не рассыпаются и, следовательно, являются полезными строительными материалами. Температуры плавления металлов сильно различаются. Ртуть при комнатной температуре находится в жидком состоянии, а щелочные металлы плавятся при температуре ниже 200 °C. Некоторые постпереходные металлы также имеют низкие температуры плавления, тогда как переходные металлы плавятся при температурах выше 1000 °C. Эти различия отражают различия в силе металлической связи между металлами.
Температуры плавления металлов сильно различаются. Ртуть при комнатной температуре находится в жидком состоянии, а щелочные металлы плавятся при температуре ниже 200 °C. Некоторые постпереходные металлы также имеют низкие температуры плавления, тогда как переходные металлы плавятся при температурах выше 1000 °C. Эти различия отражают различия в силе металлической связи между металлами.
Рисунок \(\PageIndex{4}\): Медь представляет собой твердое металлическое вещество.
Твердые вещества с ковалентной сеткой
Твердые вещества с ковалентной сеткой включают кристаллы алмаза, кремния, некоторых других неметаллов и некоторые ковалентные соединения, такие как диоксид кремния (песок) и карбид кремния (карборунд, абразив на наждачной бумаге). Многие минералы имеют сети ковалентных связей. Атомы в этих твердых телах удерживаются вместе сетью ковалентных связей, как показано на рисунке \(\PageIndex{5}\). Чтобы разорвать или расплавить твердое тело ковалентной сети, необходимо разорвать ковалентные связи. Поскольку ковалентные связи относительно прочны, твердые вещества с ковалентной сеткой обычно характеризуются твердостью, прочностью и высокими температурами плавления. Например, алмаз является одним из самых твердых известных веществ и плавится при температуре выше 3500 °C.
Поскольку ковалентные связи относительно прочны, твердые вещества с ковалентной сеткой обычно характеризуются твердостью, прочностью и высокими температурами плавления. Например, алмаз является одним из самых твердых известных веществ и плавится при температуре выше 3500 °C.
Рисунок \(\PageIndex{5}\). Ковалентный кристалл содержит трехмерную сеть ковалентных связей, о чем свидетельствуют структуры алмаза, диоксида кремния, карбида кремния и графита. Исключительным примером является графит, состоящий из плоских слоев ковалентных кристаллов, которые удерживаются вместе слоями нековалентными силами. В отличие от типичных ковалентных твердых тел, графит очень мягкий и электропроводящий. Сложная трехмерная структура алмаза, диоксида кремния, карбида кремния и графита показана вместе с меньшей повторяющейся единицей структуры, показанной над каждой структурой.
Молекулярные твердые вещества
Молекулярные твердые вещества, такие как лед, сахароза (столовый сахар) и йод, как показано на рисунке \(\PageIndex{6}\), состоят из нейтральных молекул. Величина сил притяжения между единицами, присутствующими в разных кристаллах, сильно различается, на что указывают температуры плавления кристаллов. Небольшие симметричные молекулы (неполярные молекулы), такие как H 2 , N 2 , O 2 и F 2 , обладают слабыми силами притяжения и образуют молекулярные твердые вещества с очень низкими температурами плавления (ниже -200 ° C). ). Вещества, состоящие из более крупных неполярных молекул, обладают большей силой притяжения и плавятся при более высоких температурах. Молекулярные твердые тела, состоящие из молекул с постоянными дипольными моментами (полярные молекулы), плавятся при еще более высоких температурах. Примеры включают лед (точка плавления, 0 ° C) и столовый сахар (точка плавления, 185 ° C).
Величина сил притяжения между единицами, присутствующими в разных кристаллах, сильно различается, на что указывают температуры плавления кристаллов. Небольшие симметричные молекулы (неполярные молекулы), такие как H 2 , N 2 , O 2 и F 2 , обладают слабыми силами притяжения и образуют молекулярные твердые вещества с очень низкими температурами плавления (ниже -200 ° C). ). Вещества, состоящие из более крупных неполярных молекул, обладают большей силой притяжения и плавятся при более высоких температурах. Молекулярные твердые тела, состоящие из молекул с постоянными дипольными моментами (полярные молекулы), плавятся при еще более высоких температурах. Примеры включают лед (точка плавления, 0 ° C) и столовый сахар (точка плавления, 185 ° C).
Рисунок \(\PageIndex{6}\): Двуокись углерода (CO 2 ) состоит из небольших неполярных молекул и образует молекулярное твердое вещество с температурой плавления −78 °C. Йод (I 2 ) состоит из более крупных неполярных молекул и образует молекулярное твердое вещество, которое плавится при 114 °C. Слева на трехмерном рисунке много красных и серых молекул плотно сложены друг с другом, чтобы представить углекислый газ. Справа случайным образом разбросаны фиолетовые молекулы, обозначающие йод.
Слева на трехмерном рисунке много красных и серых молекул плотно сложены друг с другом, чтобы представить углекислый газ. Справа случайным образом разбросаны фиолетовые молекулы, обозначающие йод.
Свойства твердых тел
Кристаллическое твердое тело, подобное перечисленным в таблице \(\PageIndex{1}\), имеет точную температуру плавления, поскольку каждый атом или молекула одного и того же типа удерживается на месте с одинаковыми силами или энергией. Таким образом, притяжение между единицами, составляющими кристалл, имеет одинаковую силу и требует одинакового количества энергии для разрушения. Постепенное размягчение аморфного материала резко отличается от отчетливого плавления кристаллического твердого тела. Это является следствием структурной неэквивалентности молекул в аморфном твердом теле. Одни силы слабее других, и при нагревании аморфного материала первыми разрушаются самые слабые межмолекулярные силы притяжения. При дальнейшем повышении температуры более сильные притяжения разрушаются.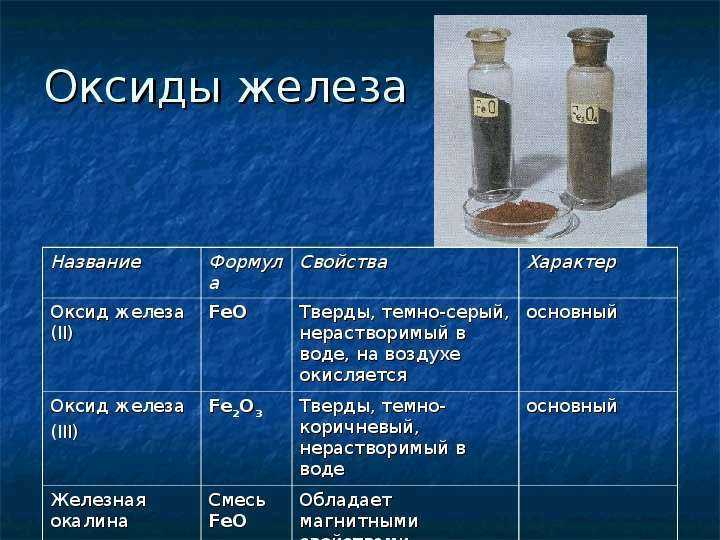 Таким образом, аморфные материалы размягчаются в диапазоне температур.
Таким образом, аморфные материалы размягчаются в диапазоне температур.
Графен: материал будущего
Углерод является важным элементом в нашем мире. Уникальные свойства атомов углерода позволяют существовать основанным на углероде формам жизни, таким как мы. Углерод образует огромное количество разнообразных веществ, которые мы используем ежедневно, включая те, что показаны на рисунке \(\PageIndex{7}\). Возможно, вы знакомы с алмазом и графитом, двумя наиболее распространенными аллотропов углерода. (Аллотропы — это разные структурные формы одного и того же элемента.) Алмаз — одно из самых твердых известных веществ, тогда как графит достаточно мягок, чтобы его можно было использовать в качестве грифеля карандаша. Эти очень разные свойства проистекают из различного расположения атомов углерода в разных аллотропах.
Уникальные свойства атомов углерода позволяют существовать основанным на углероде формам жизни, таким как мы. Углерод образует огромное количество разнообразных веществ, которые мы используем ежедневно, включая те, что показаны на рисунке \(\PageIndex{7}\). Возможно, вы знакомы с алмазом и графитом, двумя наиболее распространенными аллотропов углерода. (Аллотропы — это разные структурные формы одного и того же элемента.) Алмаз — одно из самых твердых известных веществ, тогда как графит достаточно мягок, чтобы его можно было использовать в качестве грифеля карандаша. Эти очень разные свойства проистекают из различного расположения атомов углерода в разных аллотропах.
Рисунок \(\PageIndex{7}\): Алмаз чрезвычайно тверд из-за сильной связи между атомами углерода во всех направлениях. Графит (в карандашном грифеле) стирается с бумаги из-за слабого притяжения между углеродными слоями. Изображение поверхности графита показывает расстояние между центрами соседних атомов углерода. (фото слева: модификация работы Стива Джурветсона; фото в центре: модификация работы Геологической службы США) Крупный план алмаза показывает трехмерную структуру сложной сети хорошо связанных атомов углерода. Крупный план графита показывает несколько слоев углеродных листов. Каждый лист состоит из повторяющейся и связанной гексагональной структуры атомов углерода. На третьей диаграмме видно, что расстояние между центрами атомов равно 1,4 умножить на 10 в степени минус 10 метров.
(фото слева: модификация работы Стива Джурветсона; фото в центре: модификация работы Геологической службы США) Крупный план алмаза показывает трехмерную структуру сложной сети хорошо связанных атомов углерода. Крупный план графита показывает несколько слоев углеродных листов. Каждый лист состоит из повторяющейся и связанной гексагональной структуры атомов углерода. На третьей диаграмме видно, что расстояние между центрами атомов равно 1,4 умножить на 10 в степени минус 10 метров.
Возможно, вы менее знакомы с недавно открытой формой углерода: графеном. Графен был впервые выделен в 2004 году, когда с помощью ленты снимали с графита все более тонкие слои. По сути, это один лист (толщиной в один атом) графита. Графен, показанный на рисунке \(\PageIndex{8}\), не только прочен и легок, но также является отличным проводником электричества и тепла. Эти свойства могут оказаться очень полезными в широком диапазоне приложений, таких как значительно улучшенные компьютерные микросхемы и схемы, более совершенные батареи и солнечные элементы, а также более прочные и легкие конструкционные материалы.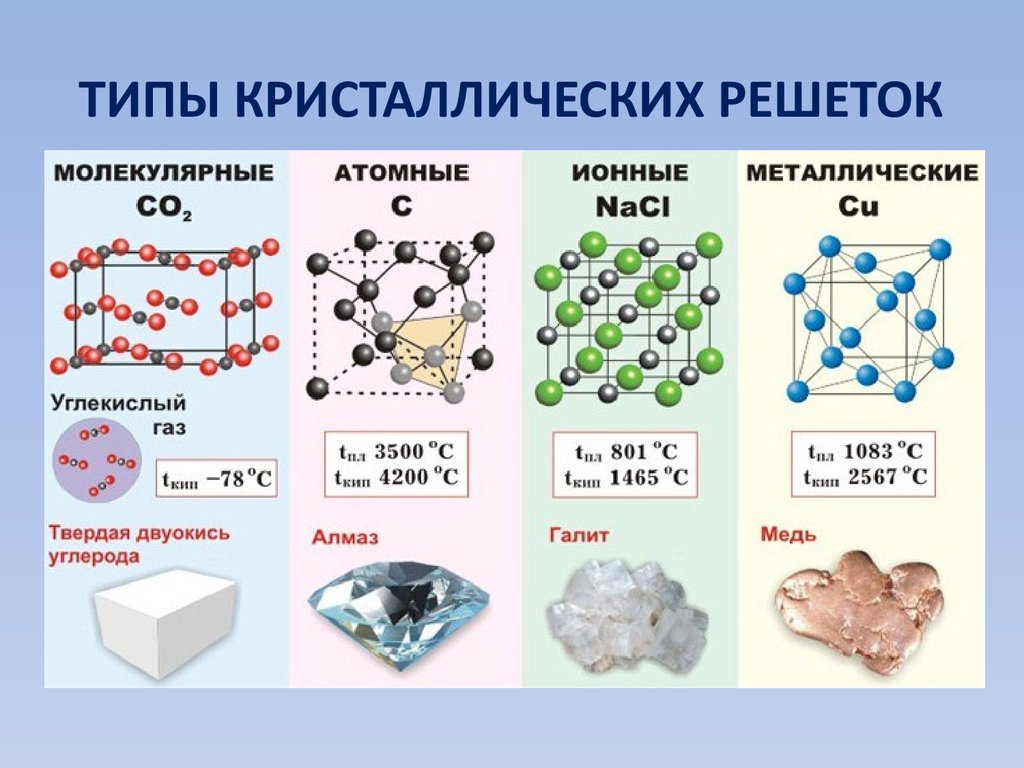 Нобелевская премия по физике 2010 года была присуждена Андрею Гейму и Константину Новоселову за их новаторскую работу с графеном.
Нобелевская премия по физике 2010 года была присуждена Андрею Гейму и Константину Новоселову за их новаторскую работу с графеном.
Рисунок \(\PageIndex{8}\): Листы графена могут быть сформированы в виде шариков, нанотрубок и сложенных друг в друга слоев. Вверху показан лист взаимосвязанных шестиугольных колец. Под ним показан bukcyball, представляющий собой сферу, состоящую из шестиугольных колец. На нижнем среднем изображении показана нанотрубка, полученная путем скручивания листа графена в трубку. На нижнем правом изображении показаны сложенные листы, состоящие из четырех горизонтальных листов, состоящих из соединенных шестиугольных колец.
Кристаллические дефекты
В кристаллическом твердом теле атомы, ионы или молекулы расположены в определенном повторяющемся порядке, но случайные дефекты могут возникать в этом порядке. Известно несколько типов дефектов, как показано на рисунке \(\PageIndex{9}\). Вакансии — это дефекты, возникающие, когда позиции, которые должны содержать атомы или ионы, являются вакантными. Реже некоторые атомы или ионы в кристалле могут занимать позиции, называемые междоузлиями, расположенные между обычными позициями для атомов. В нечистых кристаллах обнаруживаются и другие искажения, например, когда катионы, анионы или молекулы примеси слишком велики, чтобы вписаться в правильные положения без искажения структуры. Иногда к кристаллу добавляют следовые количества примесей (процесс, известный как легирование) для создания дефектов в структуре, которые приводят к желаемым изменениям ее свойств. Например, кристаллы кремния легируют различным количеством различных элементов, чтобы получить подходящие электрические свойства для их использования в производстве полупроводников и компьютерных микросхем.
Реже некоторые атомы или ионы в кристалле могут занимать позиции, называемые междоузлиями, расположенные между обычными позициями для атомов. В нечистых кристаллах обнаруживаются и другие искажения, например, когда катионы, анионы или молекулы примеси слишком велики, чтобы вписаться в правильные положения без искажения структуры. Иногда к кристаллу добавляют следовые количества примесей (процесс, известный как легирование) для создания дефектов в структуре, которые приводят к желаемым изменениям ее свойств. Например, кристаллы кремния легируют различным количеством различных элементов, чтобы получить подходящие электрические свойства для их использования в производстве полупроводников и компьютерных микросхем.
Рисунок \(\PageIndex{9}\): Типы кристаллических дефектов включают вакансии, межузельные атомы и примеси замещения.
Резюме
Некоторые вещества образуют кристаллические твердые тела, состоящие из частиц очень организованной структуры; другие образуют аморфные (некристаллические) твердые тела с неупорядоченной внутренней структурой.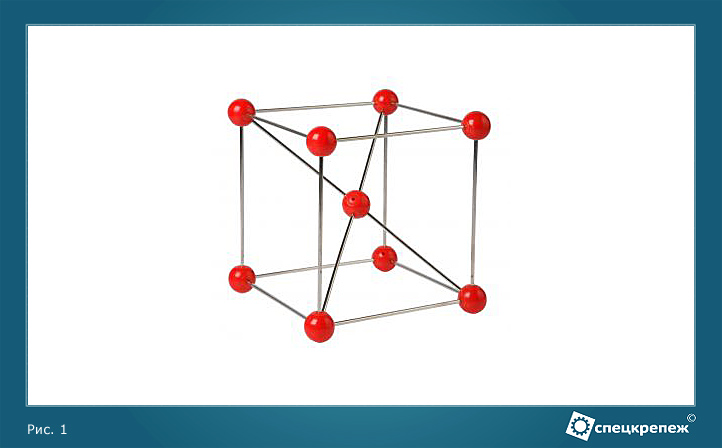 Основными типами кристаллических твердых тел являются ионные твердые тела, металлические твердые тела, твердые тела с ковалентной сеткой и молекулярные твердые тела. Свойства различных видов кристаллических твердых тел обусловлены типами частиц, из которых они состоят, расположением частиц и силой притяжения между ними. Поскольку их частицы испытывают одинаковое притяжение, кристаллические твердые тела имеют разные температуры плавления; частицы в аморфных твердых телах испытывают ряд взаимодействий, поэтому они постепенно размягчаются и плавятся в диапазоне температур. Некоторые кристаллические твердые тела имеют дефекты в определенном повторяющемся узоре их частиц. Эти дефекты (которые включают вакансии, атомы или ионы, не находящиеся в правильном положении, а также примеси) изменяют физические свойства, такие как электропроводность, которая используется в кристаллах кремния, используемых для производства компьютерных микросхем.
Основными типами кристаллических твердых тел являются ионные твердые тела, металлические твердые тела, твердые тела с ковалентной сеткой и молекулярные твердые тела. Свойства различных видов кристаллических твердых тел обусловлены типами частиц, из которых они состоят, расположением частиц и силой притяжения между ними. Поскольку их частицы испытывают одинаковое притяжение, кристаллические твердые тела имеют разные температуры плавления; частицы в аморфных твердых телах испытывают ряд взаимодействий, поэтому они постепенно размягчаются и плавятся в диапазоне температур. Некоторые кристаллические твердые тела имеют дефекты в определенном повторяющемся узоре их частиц. Эти дефекты (которые включают вакансии, атомы или ионы, не находящиеся в правильном положении, а также примеси) изменяют физические свойства, такие как электропроводность, которая используется в кристаллах кремния, используемых для производства компьютерных микросхем.
Глоссарий
- аморфное твердое вещество
- (также некристаллическое твердое вещество) твердое вещество, в котором частицы не имеют упорядоченной внутренней структуры
- сплошная ковалентная сеть
- твердое тело, частицы которого удерживаются вместе ковалентными связями
- кристаллическое твердое вещество
- твердое тело, в котором частицы расположены в определенном повторяющемся порядке
- промежуточные сайты
- промежутков между регулярными положениями частиц в любом массиве атомов или ионов 904:00
- ионное твердое вещество
- твердое тело, состоящее из положительных и отрицательных ионов, удерживаемых вместе сильным электростатическим притяжением
- сплошной металлический
- твердое тело, состоящее из атомов металла
- молекулярное твердое вещество
- твердое тело, состоящее из нейтральных молекул, удерживаемых вместе силами межмолекулярного притяжения
- вакансия
- дефект, возникающий, когда позиция, которая должна содержать атом или ион, является вакантной 904:00
Эта страница под названием 10.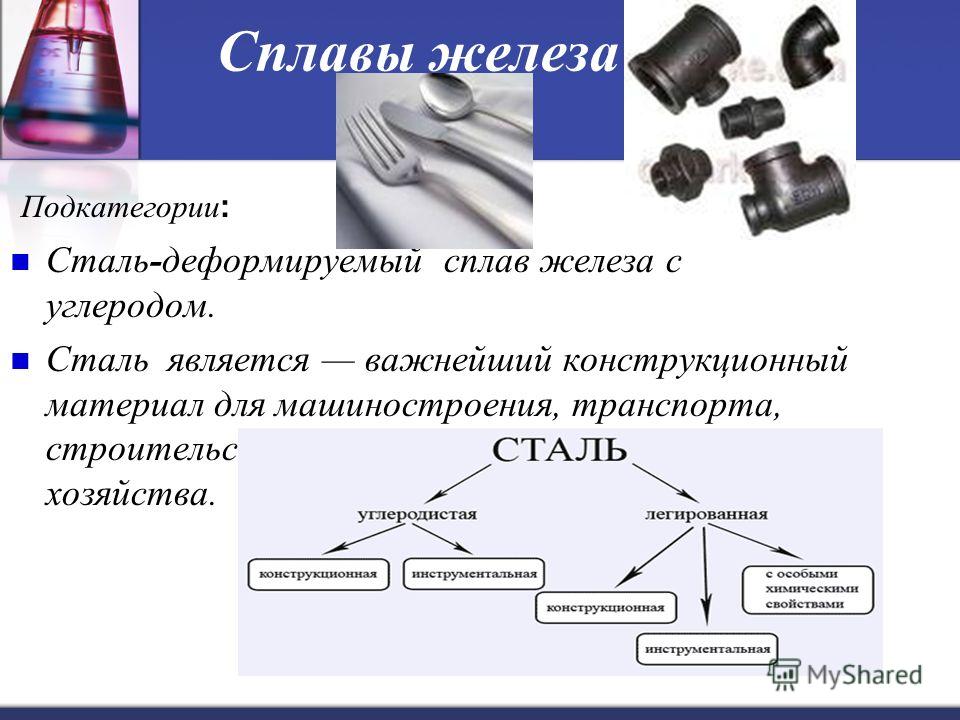 5: The Solid State of Matter распространяется под лицензией CC BY 4.0 и была создана, изменена и/или курирована OpenStax с помощью исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
5: The Solid State of Matter распространяется под лицензией CC BY 4.0 и была создана, изменена и/или курирована OpenStax с помощью исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- ОпенСтакс
- Лицензия
- СС BY
- Версия лицензии
- 4,0
- Показать страницу Содержание
- нет на странице
- Теги
- аморфное твердое вещество
- Тег автора:OpenStax
- твердая ковалентная сеть
- кристаллическое твердое вещество
- межстраничных сайтов
- ионное твердое вещество
- металлический твердый
- молекулярное твердое вещество
- источник@https://openstax.


 соединение,
соединение,