Большая Энциклопедия Нефти и Газа. Аморфное вещество это
Аморфные вещества. Кристаллическое и аморфное состояние вещества. Применение аморфных веществ
Вы когда-нибудь задумывались о том, что представляют собой загадочные аморфные вещества? По строению они отличаются и от твердых, и от жидких. Дело в том, что такие тела находятся в особом конденсированном состоянии, имеющем только ближний порядок. Примеры аморфных веществ - смола, стекло, янтарь, каучук, полиэтилен, поливинилхлорид (наши любимые пластиковые окна), различные полимеры и другие. Это твердые тела, у которых нет кристаллической решетки. Еще к ним можно отнести сургуч, различные клеи, эбонит и пластмассы.
Необыкновенные свойства аморфных веществ
Во время расщепления в аморфных телах не образуются грани. Частицы совершенно беспорядочны и находятся на близком расстоянии друг к другу. Они могут быть как сильно густыми, так и вязкими. Как на них влияют внешние воздействия? Под влиянием различных температур тела становятся текучими, словно жидкости, и одновременно довольно упругими. В случае, когда внешнее воздействие длится недолго, вещества аморфного строения могут при мощном ударе расколоться на кусочки. Длительное влияние извне приводит к тому, что они просто-напросто текут.

Попробуйте провести дома небольшой эксперимент с применением смолы. Положите ее на твердую поверхность, и вы заметите, что она начинает плавно растекаться. Правильно, ведь это аморфное вещество! Скорость зависит от показателей температуры. Если она будет сильно высокой, то растекаться смола начнет заметно быстрее.
Что еще характерно для таких тел? Они могут принимать любую форму. Если аморфные вещества в виде маленьких частиц поместить в сосуд, например, в кувшин, то они также примут форму сосуда. Еще они являются изотропными, то есть проявляют одинаковые физические свойства по всем направлениям.
Плавление и переход в другие состояния. Металл и стекло
Аморфное состояние вещества не подразумевает поддержания какой-либо определенной температуры. При низких показателях тела застывают, при высоких - плавятся. Кстати, от этого зависит и степень вязкости таких веществ. Низкая температура способствует пониженной вязкости, высокая, наоборот, ее повышает.

Для веществ аморфного типа можно выделить еще одну особенность - переход в кристаллическое состояние, причем самопроизвольный. Почему так происходит? Внутренней энергии в кристаллическом теле намного меньше, чем в аморфном. Мы это можем заметить на примере стеклянной продукции - со временем стекла становятся мутными.
Металлическое стекло - что же это такое? Металл можно избавить от кристаллической решетки в ходе плавления, то есть сделать вещество аморфного строения стеклообразным. Во время застывания при искусственном охлаждении кристаллическая решетка снова образуется. Аморфный металл имеет просто поразительную стойкость к коррозии. Например, сделанный из него кузов автомобиля не нуждался бы в различных покрытиях, так как не подвергался бы самопроизвольному разрушению. Аморфным веществом является такое тело, атомная структура которого обладает невиданной прочностью, а значит, аморфный металл мог бы применяться в совершенно любой промышленной отрасли.
Кристаллическое строение веществ
Чтобы хорошо разбираться в характеристиках металлов и уметь с ними работать, нужно обладать знаниями о кристаллическом строении тех или иных веществ. Производство продукции из металлов и область металлургии не смогли бы получить такое развитие, если бы у людей не было определенных знаний об изменениях в структуре сплавов, технологических приемах и эксплуатационных характеристиках.

Четыре состояния вещества
Общеизвестно, что существует четыре агрегатных состояния: твердое, жидкое, газообразное, плазменное. Твердые аморфные вещества могут быть и кристаллическими. При таком строении может наблюдаться пространственная периодичность в расположении частиц. Эти частицы в кристаллах могут выполнять периодическое движение. Во всех телах, которые мы наблюдаем в газообразном или жидком состоянии, можно заметить движение частиц в виде хаотичного беспорядка. Аморфные твердые вещества (например, металлы в конденсированном состоянии: эбонит, стеклянная продукция, смолы) можно называть жидкостями замороженного типа, потому что у них при изменении формы можно заметить такую характерную черту, как вязкость.
Отличие аморфных тел от газов и жидкостей
Проявления пластичности, упругости, упрочнения при деформации свойственны многим телам. Кристаллические и аморфные вещества в большей степени обладают этими характеристиками, в то время как жидкости и газы не имеют таких свойств. Но зато можно заметить, что они способствуют упругому изменению объема.
Кристаллические и аморфные вещества. Механические и физические свойства
Что собой представляют кристаллические и аморфные вещества? Как уже упоминалось выше, аморфными можно назвать те тела, которые обладают огромным коэффициентом вязкости, и при обыкновенной температуре их текучесть невозможна. А вот высокая температура, наоборот, позволяет, им быть текучими, как жидкость.

Совершенно другими представляются вещества кристаллического типа. Эти твердые тела могут иметь свою температуру плавления, зависящую от внешнего давления. Получение кристаллов возможно, если охладить жидкость. Если не принимать определенных мер, то можно заметить, что в жидком состоянии начинают возникать различные центры кристаллизации. В области, окружающей эти центры, происходит образование твердого вещества. Очень маленькие кристаллики начинают соединяться друг с другом в беспорядочном порядке, и получается так называемый поликристалл. Такое тело является изотропным.
Характеристики веществ
Что определяет физические и механические характеристики тел? Важное значение имеют атомные связи, а также тип кристаллической структуры. Кристаллам ионного типа характерны ионные связи, что означает плавный переход от одних атомов к другим. При этом происходит образование положительно и отрицательно заряженных частиц. Ионную связь мы можем наблюдать на простом примере - такие характеристики свойственны разнообразным оксидам и солям. Еще одна особенность ионных кристаллов - низкая проводимость тепла, но ее показатели могут заметно возрастать при нагревании. В узлах кристаллической решетки можно заметить различные молекулы, которые отличаются крепкой атомной связью.
Множество минералов, которые мы встречаем повсеместно в природе, имеют строение кристаллическое. И аморфное состояние вещества - это тоже природа в чистом виде. Только в этом случае тело представляет собой нечто бесформенное, а вот кристаллы могут принимать формы красивейших многогранников с наличием плоских граней, а также образовывать новые удивительной красоты и чистоты твердые тела.
Что представляют собой кристаллы? Аморфно-кристаллическая структура
Форма таких тел постоянна для определенного соединения. Например, берилл всегда выглядит как шестигранная призма. Проведите небольшой эксперимент. Возьмите небольшой кристаллик поваренной соли кубической формы (шар) и положите его в специальный раствор как можно более насыщенный той же поваренной соли. Со временем вы заметите, что этот тело осталось неизменным - оно снова приобрело форму куба или шара, которая присуща именно кристаллам поваренной соли.

Аморфно-кристаллические вещества - это такие тела, которые могут содержать в себе как аморфные, так и кристаллические фазы. Что влияет на свойства материалов такой структуры? Главным образом различное соотношение объемов и разное расположение по отношению друг к другу. Распространенными примерами таких веществ являются материалы из керамики, фарфора, ситаллы. Из таблицы свойств материалов с аморфно-кристаллической структурой становится известно, что фарфор содержит максимальный процент стеклофазы. Показатели колеблются в пределах 40-60-ти процентов. Самое низкое содержание мы увидим на примере каменного литья - меньше 5-ти процентов. При этом более высокое поглощение воды будет у керамической плитки.
Как известно, такие промышленные материалы, как фарфор, керамическая плитка, каменное литье и ситаллы, - это аморфно-кристаллические вещества, потому что содержат стекловидные фазы и одновременно кристаллы в своем составе. При этом стоит отметить, что свойства материалов не зависят от содержания в нем стеклофаз.
Аморфные металлы
Применение аморфных веществ наиболее активно осуществляется в области медицины. Например, быстро охлажденный металл активно используется в хирургии. Благодаря связанным с ним разработкам многие люди получили возможность самостоятельно передвигаться после тяжелых травм. Все дело в том, что вещество аморфной структуры является отличным биоматериалом для имплантации в кости. Полученные специальные винты, пластины, штыри, булавки внедряют при тяжелых переломах. Раньше в хирургии для таких целей применялись сталь и титан. Лишь позже было замечено, что аморфные вещества очень медленно распадаются в организме, а это удивительное свойство дает возможность восстановиться костным тканям. Впоследствии вещество заменяется костью.
Применение веществ аморфного типа в метрологии и точной механике
Точная механика основана именно на точности, а потому так и называется. Особенно важную роль в данной отрасли, равно как и в метрологии, играют сверхточные показатели приборов измерения, этого позволяет добиться использование в устройствах аморфных тел. Благодаря точным измерениям проводятся лабораторные и научные исследования в институтах в области механики и физики, происходит получение новых препаратов, совершенствование научных знаний.

Полимеры
Еще один пример применения аморфного вещества - это полимеры. Они могут медленно переходить из твердого состояния в жидкость, в то время как кристаллические полимеры характеризуются температурой плавления, а не температурой размягчения. Каково физическое состояние аморфных полимеров? Если предоставить этим веществам низкую температуру, можно заметить, что они будут находиться в стеклообразном состоянии и проявлять свойства твердых тел. Постепенное нагревание способствует тому, что полимеры начинают переходить в состояние повышенной эластичности.
Аморфные вещества, примеры которых мы сейчас приводили, интенсивно используются в промышленности. Сверхэластичное состояние позволяет полимерам как угодно деформироваться, а достигается такое состояние благодаря повышенной гибкости звеньев и молекул. Дальнейшее повышение показателей температуры приводит к тому, что полимер приобретает еще более эластичные свойства. Он начинает переходить в особое текучее и вязкое состояние.
Если оставить ситуацию без контроля и не воспрепятствовать дальнейшему повышению температуры, полимер подвергнется деструкции, то есть разрушению. Вязкое состояние показывает, что все звенья макромолекулы очень подвижны. Когда течет молекула полимера, звенья не только выпрямляются, но и еще и сильно сближаются друг с другом. Межмолекулярное воздействие превращает полимер в жесткое вещество (резину). Такой процесс называют механическим стеклованием. Полученное вещество используют для производства пленок и волокон.
На основе полимеров можно получить полиамиды, полиакрилонитрилы. Чтобы изготовить полимерную пленку, нужно продавить полимеры через фильеры, которые имеют щелевидное отверстие, и нанести на ленту. Таким образом изготавливаются упаковочные материалы и основы для магнитных лент. К полимерам относятся также различные лаки (образующие пенку в органическом растворителе), клеи и другие скрепляющие материалы, композиты (полимерная основа с наполнителем), пластмассы.

Области применения полимеров
Такого вида аморфные вещества прочно внедрились в нашу жизнь. Применяются они повсюду. К ним относят:
1. Различные основы для изготовления лаков, клея, пластмассовых изделий (фенолформальдегидные смолы).
2. Эластомеры или синтетические каучуки.
3. Электроизоляционный материал - поливинилхлорид, или всем известные пластиковые окна из ПВХ. Он устойчив к пожарам, так как считается трудногорючим, обладает повышенной механической прочностью и электроизоляционными свойствами.
4. Полиамид - вещество, обладающее очень высокой прочностью, стойкостью к износу. Ему свойственны высокие диэлектрические характеристики.
5. Плексиглас, или полиметилметакрилат. Его мы можем применять в сфере электротехники или использовать как материал для конструкций.
6. Фторопласт, или политетрафторэтилен, - известный диэлектрик, который не проявляет свойств растворения в растворителях органического происхождения. Обширный диапазон температур и хорошие диэлектрические свойства позволяют применять его как гидрофобный или антифрикционный материал.
7. Полистирол. Этот материал не подвержен воздействию кислот. Он, так же как фторопласт и полиамид, может считаться диэлектриком. Очень прочен в отношении механического воздействия. Полистирол используют повсеместно. Например, он хорошо зарекомендовал себя как конструкционный и электроизоляционный материал. Применяется в электро- и радиотехнике.
8. Наверное, самый известный для нас полимер - это полиэтилен. Материал проявляет устойчивость при воздействии агрессивной среды, он абсолютно не пропускает влагу. Если упаковка выполнена из полиэтилена, можно не бояться, что содержимое испортится под воздействием сильного дождя. Полиэтилен - это тоже диэлектрик. Его применение обширно. Из него изготавливают трубные конструкции, различные электротехнические изделия, изоляционную пленку, оболочки для кабелей телефонных и силовых линий, детали для радио и другой аппаратуры.
9. Полихлорвинил - это высокополимерное вещество. Он является синтетическим и термопластичным. Обладает структурой молекул, которые несимметричны. Почти не пропускает воду и изготавливается путем прессования с помощью штамповки и путем формования. Полихлорвинил применяют чаще всего в электрической промышленности. На его основе создают различные теплоизоляционные шланги и шланги для химической защиты, аккумуляторные банки, изоляционные втулки и прокладки, провода и кабели. Полихлорвинил также является отличной заменой вредному свинцу. Его нельзя применять в качестве высокочастотных цепей в виде диэлектрика. А все из-за того, что в этом случае показатели диэлектрических потерь будут высокими. Обладает высокой проводимостью.
fb.ru
Аморфные тела
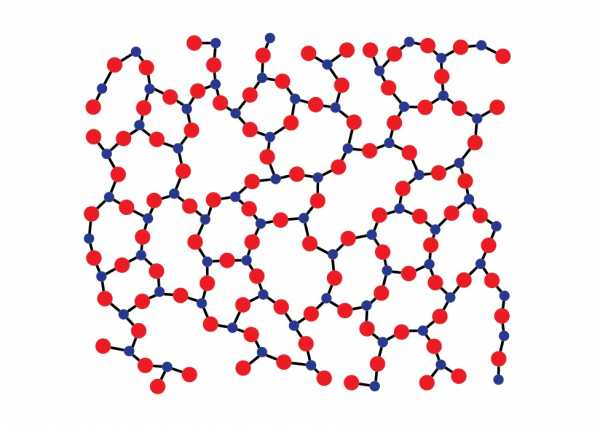
Аморфные тела (структура диоксида кремния)
Твердые тела разделяют на аморфные и кристаллические, в зависимости от их молекулярной структуры и физических свойств.
В отличие от кристаллов молекулы и атомы аморфных твердых тел не формируют решетку, а расстояние между ними колеблется в пределах некоторого интервала возможных расстояний. Иначе говоря, у кристаллов атомы или молекулы взаимно расположены таким образом, что формируемая структура может повторяться во всем объеме тела, что называется дальним порядком. В случае же с аморфными телами – сохраняется структура молекул лишь относительно каждой одной такой молекулы, наблюдается закономерность в распределении только соседних молекул – ближний порядок. Наглядный пример представлен ниже.
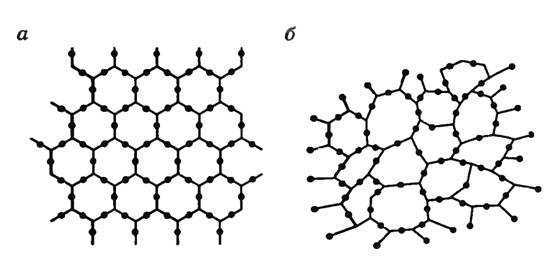
На рисунке слева (а) изображена решетка молекул кварца, а справа (б) расположение молекул кварцевого стекла, которое является аморфным телом.
К аморфным телам относится стекло и другие вещества в стеклообразном состоянии, канифоль, смолы, янтарь, сургуч, битум, воск, а также органические вещества: каучук, кожа, целлюлоза, полиэтилен и др.
Свойства аморфных тел
Особенность строения аморфных твердых тел придает им индивидуальные свойства:
- Слабо выраженная текучесть – одно из наиболее известных свойств таких тел. Примером будут потеки стекла, которое долгое время стоит в оконной раме.
- Аморфные твердые тела не обладают определенной температурой плавления, так как переход в состояние жидкости во время нагрева происходит постепенно, посредством размягчения тела. По этой причине к таким телам применяют так называемый температурный интервал размягчения.
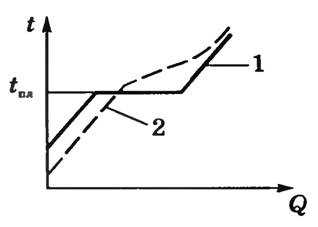
График перехода аморфного тела в жидкое состояние изображен пунктирной линией (2), а график перехода обычного твердого тела в жидкое состояние – сплошной (1).
- В силу своей структуры такие тела являются изотропными, то есть их физические свойства не зависят от выбора направления.
- Вещество в аморфном состоянии обладает большей внутренней энергией, нежели в кристаллическом. По этой причине аморфные тела способны самостоятельно переходить в кристаллическое состояние. Данное явление можно наблюдать как результат помутнения стекол с течением времени.
Стеклообразное состояние
В природе существуют жидкости, которые практически невозможно перевести в кристаллическое состояние посредством охлаждения, так как сложность молекул этих веществ не позволяет им образовать регулярную кристаллическую решетку. К таким жидкостям относятся молекулы некоторых органических полимеров.
Материалы по теме

Однако, при помощи глубокого и быстрого охлаждения, практически любое вещество способно перейти в стеклообразное состояние. Это такое аморфное состояние, которое не имеет явной кристаллической решетки, но может частично кристаллизироваться, в масштабах малых кластеров. Данное состояние вещества является метастабильным, то есть сохраняется при некоторых требуемых термодинамических условиях.
При помощи технологии охлаждения с определенной скоростью вещество не будет успевать кристаллизоваться, и преобразуется в стекло. То есть чем выше скорость охлаждения материала, тем меньше вероятность его кристаллизации. Так, например, для изготовления металлических стекол потребуется скорость охлаждения, равная 100 000 – 1 000 000 Кельвин в секунду.
В природе вещество существует в стеклообразном состоянии возникает из жидкой вулканической магмы, которая, взаимодействуя с холодной водой или воздухом, быстро охлаждается. В данном случае вещество зовется вулканическим стеклом. Также можно наблюдать стекло, образованная в результате плавления падающего метеорита, взаимодействующего с атмосферой – метеоритное стекло или молдавит.

Молдавит, естественное стекло, образованное ударом метеорита, из Беседин, Богемия, Чехия.
comments powered by HyperComments
Понравилась запись? Расскажи о ней друзьям!
Просмотров записи: 3383
spacegid.com
Аморфные вещества Википедия

Амо́рфные вещества́ (тела́) (от др.-греч. ἀ «не-» + μορφή «вид, форма») — конденсированное состояние веществ, атомная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, (если не были под сильнейшим анизотропным воздействием — сжатием или электрическим полем, например) обладают изотропией свойств, то есть не обнаруживают различия свойств в разных направлениях. Аморфные вещества не имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования (Tg) переходят в жидкое состояние. Вещества, обычно имеющие (поли-)кристаллическую структуру, но сильно переохлаждённые при затвердевании, могут затвердевать в аморфном состоянии, которое при последующем нагреве или с течением времени кристаллизуется (в твёрдом состоянии с небольшим выделением тепла).
Аморфное состояние многих веществ получается при высокой скорости затвердевания (остывания) жидкого расплава, или при конденсации паров на охлаждённую заметно ниже температуры плавления поверхность-подложку. Соотношение реальной скорости охлаждения (dT/dt) и характеристической скорости кристаллизации определяет долю поликристаллов в аморфном объёме. Скорость кристаллизации — параметр вещества, слабо зависящий от давления и от температуры (около точки плавления) и сильно зависящий от сложности состава. У металлов и сплавов аморфное состояние формируется, как правило, если расплав охлаждается за время порядка сотни и тысячи лет; для стёкол достаточно намного меньшей скорости охлаждения — долей-десятков миллисекунд . Кварц (SiO2) также имеет низкую скорость кристаллизации, поэтому отлитые из него изделия получаются аморфными. Однако природный кварц, имевший сотни и тысячи лет для кристаллизации при остывании земной коры или глубинных слоёв вулканов, имеет крупнокристаллическое строение, в отличие от вулканического стекла, застывшего на поверхности и поэтому аморфного.
Из обычных полимеров (пластмасс) только самый простой (полиэтилен) имеет заметную скорость кристаллизации при комнатной температуре — порядка двух лет для мягкого (ПВД) и нескольких лет (даже с добавками-замедлителями) для твёрдого (ПНД) — уже примерно наполовину кристаллизованного вида. Это одна из причин недолговечности изделий из полиэтилена.
К стабильно-аморфным веществам принадлежат стекла (искусственные и вулканические), естественные и искусственные смолы, клеи, парафин, воск и др. Аморфные вещества могут находиться либо в стеклообразном состоянии (при низких температурах), либо в состоянии расплава (при высоких температурах). Аморфные вещества переходят в стеклообразное состояние при температурах заметно ниже температуры стеклования Tg. При температурах намного выше Tg аморфные вещества ведут себя как расплавы, то есть находятся в расплавленном состоянии. Вязкость аморфных материалов — непрерывная функция температуры: чем выше температура, тем ниже вязкость аморфного вещества.
Структура
Исследования показали, что структуры жидкостей и аморфных тел имеют много общего. В аморфных и жидких телах наблюдается ближний порядок в упаковке частиц (атомов или молекул).
Также бывают промежуточные полуаморфные (полукристаллические) состояния.
Свойства
Все физические свойства аморфного и поликристаллического состояний одного и того же вещества заметно (иногда сильно) отличаются (кроме плотности).
Электрические и механические свойства аморфных веществ ближе к таковым для монокристаллов, чем для поликристаллов из-за отсутствия резких и сильно загрязнённых примесями межкристаллических границ с зачастую абсолютно другим химическим составом. Немеханические свойства полуаморфных состояний обычно являются промежуточными между аморфными и кристаллическими и изотропны.
При внешних воздействиях аморфные вещества обнаруживают одновременно упругие свойства, подобно кристаллическим твёрдым веществам, и текучесть, подобно жидкости, поэтому моделируются в механике сплошных сред как вязкоупругие среды. Так, при кратковременных воздействиях (ударах) они ведут себя как твёрдые вещества и при сильном ударе раскалываются на куски. Но при очень продолжительном воздействии (например растяжении) аморфные вещества текут. Например, аморфным веществом также является смола (или гудрон, битум). Если раздробить её на мелкие части и получившейся массой заполнить сосуд, то через некоторое время смола сольётся в единое целое и примет форму сосуда.
В зависимости от электрических свойств, разделяют аморфные металлы, аморфные неметаллы и аморфные полупроводники.
Литература
- Скрышевский А. Ф. Структурный анализ жидкостей и аморфных тел. — 2-е изд., перераб. и доп.. — М.: Высшая школа, 1980. — С. 302-324. — 328 с.
- Шульц М. М., Мазурин О. В. Современное представление о строении стёкол и их свойствах. — Л.: Наука. 1988. — 200 с. — ISBN 5-02-024564-X.
См. также
wikiredia.ru
Аморфные тела - это... Что такое Аморфные тела?
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 12 ноября 2012. |
.
Сравнение атомарной решетки кристаллов и аморфных телАмо́рфные вещества́ (тела́) (от др.-греч. ἀ «не-» и μορφή «вид, форма») — конденсированное состояние вещества, атомарная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, (если не были под сильнейшим анизотропным воздействием — сжатием или электрическим полем, например) обладают изотропией свойств, то есть не обнаруживают различных свойств в разных направлениях. И не имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования (Tg) переходят в жидкое состояние. Вещества с высокой скоростью кристаллизации, обычно имеющие (поли-)кристаллических структуру, но сильно переохлаждённые при затвердевании в аморфное состояние, при последующем нагреве незадолго до плавления рекристаллизуются (в твёрдом состоянии с небольшим выделением тепла), а затем плавятся как обычные поликристаллические.
Получаются при высокой скорости затвердевания(остывания) жидкого расплава или конденсацией паров на охлаждённую заметно ниже температуры ПЛАВЛЕНИЯ(не кипения!) подложку(любой предмет). Соотношение реальной скорости охлаждения (dT/dt) и характеристической скорости кристаллизации определяет долю поликристаллов в аморфном объёме. Скорость кристаллизации — параметр вещества, слабо зависящий от давления и от температуры (около точки плавления — сильно). И сильно зависящий от сложности состава — для металлов порядка долей-десятков миллисекунд; а для стёкол при комнатной температуре — сотни и тысячи лет (старые стёкла и зеркала мутнеют).
Кварц (SiO2) также имеет низкую скорость кристаллизации, поэтому отлитые из него изделия получаются аморфными. Однако природный кварц, имевший сотни и тысячи лет для кристаллизации при остывании земной коры или глубинных слоев вулканов, имеет крупнокристаллическое строение, в отличие от вулканического стекла, застывшего на поверхности.
Из обычных полимеров (пластмасс) только (самый простейший) полиэтилен имеет заметную скорость кристаллизации - порядка двух лет для мягкого (ПНД) и нескольких лет (даже с добавками-замедлителями) для твёрдого (ПВД — уже примерно наполовину кристаллизованного) видов. Это одна из причин недолговечности изделий из полиэтилена.
К стабильно-аморфным веществам принадлежат стекла (искусственные и вулканические), естественные и искусственные смолы, клеи, парафин, воск и др. Аморфные вещества могут находиться либо в стеклообразном состоянии (при низких температурах), либо в состоянии расплава (при высоких температурах). Аморфные вещества переходят в стеклообразное состояние при температурах заметно ниже температуры стеклования Tg. При температурах намного выше Tg аморфные вещества ведут себя как расплавы, то есть находятся в расплавленном состоянии(если не разлагаются от перегрева и не сгорают, конечно). Вязкость аморфных материалов — непрерывная функция температуры: чем выше температура, тем ниже вязкость аморфного вещества.
Структура
Исследования показали, что структуры жидкостей и аморфных тел имеют много общего. В аморфных и жидких телах наблюдается ближний порядок в упаковке частиц (атомов или молекул). По этой причине принято считать аморфные тела очень густыми/вязкими (застывшими) жидкостями.
Также бывают промежуточные полуаморфные (полукристаллические) состояния.
Свойства
Все физические свойства аморфного и поликристаллического состояний одного и того же вещества заметно (иногда сильно) отличаются (кроме плотности).
Электрические и механические свойства аморфных веществ ближе к таковым для монокристаллов, чем для поликристаллов из-за отсутствия резких и сильно загрязнённых примесями межкристаллических переходов(границ) с зачастую абсолютно другим химическим составом.
Немеханические свойства полуаморфных состояний обычно являются промежуточными между аморфным и кристаллическим и изотропны. Однако отсутствие резких межкристаллических переходов заметно влияет на электрические и механические свойства, делая их похожими на аморфные.
При внешних воздействиях аморфные вещества обнаруживают одновременно упругие свойства, подобно кристаллическим твердым веществам, и текучесть, подобно жидкости. Так, при кратковременных воздействиях (ударах) они ведут себя как твёрдые вещества и при сильном ударе раскалываются на куски. Но при очень продолжительном воздействии (например растяжении) аморфные вещества текут. Например, аморфным веществом также является смола (или гудрон, битум). Если раздробить её на мелкие части и получившейся массой заполнить сосуд, то через некоторое время смола сольётся в единое целое и примет форму сосуда.
В зависимости от электрических свойств, разделяют аморфные металлы, аморфные неметаллы, и аморфные полупроводники.
См. также
(устаревший термин)dic.academic.ru
Аморфные вещества
Контактная линза
А вот в аморфных твердых телах такого порядка нет. В них отсутствует атомная или молекулярная решетка, характерная для веществ в кристаллическом состоянии. Частицы расположены хаотично. Это определяет их физические свойства. Например, у аморфных веществ нет определенной температуры плавления. При нагревании они размягчаются и переходят в текучее состояние. К аморфным веществам можно отнести шоколад, который тает во рту и в руках, пластилин, жевательную резинку, пластмассы, воск.
Контактные линзы изготавливают из полимеров. Так называют вещества, состоящие из большого числа повторяющихся одинаковых или различных по строению атомных группировок — составных звеньев, соединенных между собой в длинные цепочки — макромеры. Такое звено подобно элементарной ячейке в кристаллах и называется мономером. В материале для линз содержится силикон, состоящий как раз из таких длинных молекулярных цепочек. Поскольку эти цепочки расположены хаотично, силикон относят к аморфным веществам.
Примерно так выглядит аморфное вещество «изнутри», на атомном уровне
Стекло, из которого изготовлен стакан, относится к аморфным веществам. Тем не менее у него немало общего с водой, которую в него наливают. У жидкостей, как и у аморфных веществ, упорядоченность в расположении их атомов и молекул наблюдается только на малых расстояниях (что называется ближним порядком). Эти частицы очень часто перескакивают из одного положения в другое, что обусловливает их текучесть.
Различия в свойствах жидкого и твердого аморфных веществ (воды и стекла в нашем примере) связаны с характером теплового движения частиц: в аморфном состоянии частицы способны лишь к колебательным и вращательным движениям, но не могут перемещаться внутри вещества.
Поделиться ссылкой
sitekid.ru
Аморфное вещество - Большая Энциклопедия Нефти и Газа, статья, страница 1
Аморфное вещество
Cтраница 1
Аморфные вещества постепенно самопроизвольно превращаются в кристаллические, противоположный процесс ( при той же температуре) не наблюдается. Следовательно, кристаллическое состояние является равновесным и наиболее устойчивым состоянием твердого вещества. [1]
Аморфные вещества менее устойчивы, чем кристаллические. Любое аморфное вещество в принципе должно кристаллизоваться, и этот процесс должен быть экзотермическим. Так, теплоты образования аморфной и кристаллической модификаций BjCb из простых веществ равны соответственно - 1254 и - 1273 кДж / моль. Этот пример подтверждает также сравнительно небольшое различие в структуре кристаллов и аморфных веществ, а одинаковый порядок значений теплоты перехода из аморфного в кристаллическое состояние ( в данном примере она равна - 19 кДж / моль) с теплотами кристаллизации подтверждает сходство аморфного состояния с жидким. [3]
Аморфные вещества изотропны, т.е. имеют одинаковые свойства во всех направлениях. Кроме того, аморфные вещества плавятся не при строго определенной температуре, а в некотором температурном интервале. [4]
Аморфные вещества не имеют определенной температуры плавления. В отличие от кристаллов у них наблюдается растянутый интервал размягчения, в котором тело постепенно переходит из твердого состояния в жидкое. Это объясняется прежде всего неодинаковым построением элементов твердых кристаллических и аморфных тел при затвердевании. [5]
Аморфные вещества, подобно газам и жидкостям, вследствие беспорядочного расположения молекул изотропны. Кристаллы же обычно анизотропны: их физические свойства не одинаковы в различных направлениях. [6]
Аморфные вещества, обладающие большим запасом энергии, чем соответствующие им кристаллические, естественно обнаруживают и большую склонность к взаимодействию в твердом состоянии, чем эти последние. Различная склонность к взаимодействию в твердом состоянии может быть обнаружена, как это показано Хедвалом [ III-357 ], и у разных модификаций одного и того же вещества. В известных условиях различия такого рода также могут быть установлены при помощи кривых нагревания. [7]
Аморфные вещества постепенно самопроизвольно превращаются в кристаллические, противоположный процесс ( при той же температуре) не наблюдается. Следовательно, кристаллическое состояние является равновесным и наиболее устойчивым состоянием твердого вещества. [8]
Аморфное вещество рассматривают как переохлажденную жидкость с очень большим внутренним трением. Отдельные атомы или молекулы в аморфном веществе расположены беспорядочно. Аморфное вещество не обладает определенной температурой плавления. При нагревании оно все более и более размягчается, пока окончательно не расплавляется. Температура при этом непрерывно поднимается. [9]
Аморфные вещества не имеют резкой границы плавления. [10]
Аморфные вещества не имеют резкой границы плавления. [11]
Аморфные вещества отличаются от кристаллических прежде всего изотропностью. Изотропность характеризуется одинаковыми значениями данного свойства при измерении в любом направлении внутри вещества. Вторым характерным свойством аморфного вещества является то, что переход аморфного вещества из твердого состояния в жидкое не сопровождается скачкообразным изменением свойств. Этот интервал в зависимости от природы вещества может иметь значение порядка десятков и даже сотен градусов. [13]
Аморфные вещества постепенно самопроизвольно превращаются в кристаллические, противоположный процесс ( при той же температуре) не наблюдается. Следовательно, кристаллическое состояние является равновесным и наиболее устойчивым состоянием твердого вещества. [14]
Аморфные вещества, к которым относятся и каучуки, характеризуются наличием ближнего порядка и отсутствием дальнего, не имеют определенной температуры плавления, а размягчаются в некотором температурном интервале. Если аморфное вещество построено из полимерных молекул с определенным чередованием связей, то между истинно твердым состоянием ( стеклом) и текучей жидкостью существует такое состояние вещества, при котором фрагменты полимерных цепей уже могут вращаться вокруг некоторых связей, но молекулы еще не могут перемещаться относительно друг друга. В этих условиях энтропийный фактор заставляет полимерные молекулы скручиваться в клубок. Распрямление клубка, как и любое другое искажение формы, происходит без изменения длин и энергий связей, а только за счет изменения углов между фрагментами, и поэтому требует лишь небольших усилий. После снятия усилия система возвращается в исходное максимально неупорядоченное состояние. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Ответы@Mail.Ru: Какие есть виды аморфных веществ? Примеры? Жидкие кристалы
Примерами изоморфных веществ являются стекло, смола, клей. При низкой температуре аморфные вещества пребывают в стеклообразном состоянии, а при высокой температуре в состоянии расплава. Аморфные вещества обладают вязкостью. Вязкость аморфных веществ зависит от температуры: при высоких температурах аморфные вещества обладают низкой вязкостью, а при низких температурах вязкость аморфных веществ возрастает. Аморфные вещества не образуют правильной геометрической структуры, представляя собой структуры неупорядоченно расположенных молекул. В отличие от кристаллических веществ, имеющих вполне определенную температуру плавления, аморфные вещества плавятся в широком интервале температур. При нагревании они постепенно размягчаются, затем начинают растекаться и, наконец, становятся жидкими. Примерами аморфных веществ могут быть стекла и смолы. К аморфным веществам относится также большинство полимеров. Некоторые вещества могут находиться и в кристаллическом, и в аморфном состояниях, - например сера, оксид кремния ( IV ) и др.
жидкие кристаллы- не аморфное вещество. это криссталические вещества, которые при определенной, свойственной им температуре перехода образуют мутную жидкую фазу, а затем окончательно плавятся, давая прозрачные жидкости.
touch.otvet.mail.ru