Содержание
Принцип работы и устройство автомобильного катализатора
Требования к экологической чистоте транспорта становятся все жестче, поэтому инженеры автопроизводителей работают над улучшением устройств, отвечающих за очистку выхлопных газов. Одним из них стал катализатор, устройство и принцип работы которого будет рассматриваться далее. Это ответ на все рассуждения по поводу того, что можно оптимизировать качество моторного масла, топлива, рассчитывать оптимальную смесь, при которой происходит лучшее сгорание, но для этих улучшений в какой-то момент приходит предел.
Устройство катализатора
Особенности конструкции
Принцип работы
Классификация
Срок службы катализатора
Удалить катализатор: можно или нет
Самостоятельная диагностика работы катализатора
Ужесточение требований к составу выхлопных газов, образующихся при полноценной работе двигателя внутреннего сгорания, приводит к необходимости использовать более прогрессивные решения для очистки. В состав современной выхлопной системы обязательно входят элементы системы дополнительной очистки: сажевый фильтр, нейтрализатор, система дожига топлива. Их задача состоит в минимизации вредных соединений, которые выбрасываются ТС в атмосферу во время движения.
В состав современной выхлопной системы обязательно входят элементы системы дополнительной очистки: сажевый фильтр, нейтрализатор, система дожига топлива. Их задача состоит в минимизации вредных соединений, которые выбрасываются ТС в атмосферу во время движения.
Катализатор представляет собой компонент, необходимый для нейтрализации вредных соединений, являющихся составными частями выхлопов. При сгорании топлива формируются углеводороды, окрашивающие выходящие газы в темный цвет, оксидов азота и углерода. Эти соединения и вызывают у экологов негативные реакции.
Работа нейтрализатора, изначально присутствующего в выхлопной системе, направлена на окислительно-восстановительные химические реакции, приводящие к образованию безвредных веществ: воды, углекислого газа и азота. Это треступенчатые нейтрализаторы, которые и используются в большинстве автомобилей последних моделей. Принцип работы автомобильного катализатора обеспечивает превращение опасных для экологии газов в безопасные соединения, выходящие в атмосферу.
Работа нейтрализатора не требует каких-то вспомогательных источников энергии, так как активное покрытие обеспечивает протекание любых реакций. Рабочая температура элемента достаточно высокая, поэтому он находится за выпускным коллектором, но не слишком близко к мотору, чтобы не перегреваться. Такое расположение обеспечивает выход на рабочий режим за счет разогрева раскаленными выхлопными газами.
Принцип работы катализатора обеспечивает его полноценное функционирование после полного прогревания. Контролировать его работу должны лямбда-зонды – датчики кислорода, установленные перед входом в катализатор и после выхода из него. Для электронного блока управления важной является информация по количеству остаточного кислорода в выхлопе, по которому делаются выводы о функционировании мотора. Если требуется коррекция, то ЭБУ передает сигнал на увеличение или уменьшение воздушной и топливной подачи в систему камер сгорания.
Особенности конструкции
Если принцип работы катализатора выхлопных газов понятен, то можно сказать несколько слов об его устройстве. Нейтрализатор состоит из нескольких ключевых компонентов:
Нейтрализатор состоит из нескольких ключевых компонентов:
- Сразу за выпускным коллектором размещен цельный стальной корпус, внутри которого есть термоизолирующий слой, защищающий основной компонент.
- Нейтрализатор имеет наполнитель в виде сотовой структуры, покрытой внутри активным слоем. В зависимости от производителя устройства в качестве каталитического вещества может использоваться родий, платина, палладий, платиново-иридиевый сплав. Сотовая структура обеспечивает повышение площади контакта газов с активным вещество, поэтому химические реакции проходят более интенсивно.
- Наполнитель изготовлен из металла или керамики. Выбор материала зависит от конструкции и конечной стоимости оборудования.
Принцип работы
Принцип работы катализатора в автомобиле достаточно прост и базируется на определенной последовательности химических реакций:
- Внутренняя поверхность сот покрыта драгоценными металлами, которые отвечают за активацию процессов окисления.

- Оксид азота в результате реакции разлагается на атомы азота и кислорода. Азот объединяется в молекулы, образуя устойчивый азот. Кислород соединяется с угарным газом до образования углекислого газа.
- Катализатор захватывает из выхлопных газов остаточный кислород, расщепляет углеводороды, давая на выходе такие соединения, как углекислый газ и вода.
- Остаточный кислород на выходе из катализатора фиксируется лямбда-зондом, чтобы передать сведения о работе устройства штатному бортовому компьютеру.
Исправное устройство в оптимальных условиях не накапливает ничего внутри себя: все вещества, которые поступают в нейтрализатор, покидают его сотовую структуру. Но добиться этого практически невозможно, поэтому со временем происходит деградация каталитического нейтрализатора, что не дает ему полноценно справляться с задачей.
Классификация
Катализаторы можно разделить на категории по функциональности: на двух- и трехкомпонентные. Первый тип работает только с обезвреживанием угарного газа с углеводородами. Такие модели считаются устаревшими, поэтому не устанавливаются на автомобилях новых версий. Трехкомпонентные обеспечивают нейтрализацию оксида азота. Этот вид теперь устанавливается на всех современных автомобилях.
Первый тип работает только с обезвреживанием угарного газа с углеводородами. Такие модели считаются устаревшими, поэтому не устанавливаются на автомобилях новых версий. Трехкомпонентные обеспечивают нейтрализацию оксида азота. Этот вид теперь устанавливается на всех современных автомобилях.
Если говорить о материале изготовления, то принято выделять керамические, металлические и спортивные:
- Керамические считаются самыми дешевыми, но это и наиболее хрупкие катализаторы. При ударе по корпусу происходит разрушение сердцевины. Устройства страдают от перепадов температур, сбоев в системе зажигания авто. Катализатор может постепенно разрушаться, что приводит к образованию большого количества мелкой пыли, которая проникает сквозь выпускной коллектор в мотор, что приводит к поломкам. В результате всех этих неполадок может потребоваться капитальный ремонт.
- Металлические – это дорогие, но надежные устройства, изготовленные из металлической структуры в виде сот. Она отличается упругостью и устойчивостью к механическим и температурным воздействиям.
 Металл не способен образовывать мелкие частицы, поэтому для двигателя он не представляет опасности.
Металл не способен образовывать мелкие частицы, поэтому для двигателя он не представляет опасности. - Спортивные отличаются повышенной пропускной способностью, поэтому мотор становится мощнее на несколько процентов. Спортивные монтируются в прямоточные системы выхлопных газов. Их считают наиболее надежными, хоть они и самые дорогостоящие.
Срок службы катализатора
Для катализатора средний ресурс составляет 100 тысяч километров пробега, но в условиях правильной эксплуатации он способен исправно отработать до 200 тысяч. Ранний износ может произойти из-за низкого качества топлива (топливно-воздушной смеси) и проблем с мотором.
Если топливная смесь обедненная, то случается перегрев нейтрализатора, если слишком богатая, то это приводит к засорению пористого блока остатками несгоревшего топлива, из-за чего не протекают необходимые химические реакции. Это вызывает проблемы в работе катализатора с его ускоренным выходом из строя.
Механические повреждения тоже часто приводят к возникновению неисправностей. Удары и различные механические воздействия приводят к возникновению трещин. Это становится причиной стремительного разрушения блоков.
Удары и различные механические воздействия приводят к возникновению трещин. Это становится причиной стремительного разрушения блоков.
Если возникает любая неисправность, каталитический нейтрализатор начинает хуже работать, что можно понять по показаниям, поступающим в ЭБУ от лямбда-зонда, установленного на выходе из нейтрализатора. Сообщение о неисправности может высвечиваться на приборной панели в виде ошибки «Check Engine». Помимо этого, о выходе из строя свидетельствует ухудшение динамики, увеличение топливного расхода и дребезжание при движении.
В такой ситуации требуется его замена на новый. При этом можно установить новый оригинальный компонент либо воспользоваться универсальным. Восстановление или чистка не возможны, а так как новый компонент обычно стоит довольно дорого, многие автовладельцы предпочитают удалить его.
Удалить катализатор: можно или нет
Так как повлиять на принцип работы датчика катализатора невозможно, и он будет выдавать ошибку, если компонент вышел из строя, то многие автовладельцы предпочитают использовать альтернативные довольно радикальные подходы. Чаще всего просто удаляют катализатор, а на его место устанавливают пламегаситель, который выравнивает поток выхлопных газов. Его рекомендуется использовать для устранения неприятных шумов, сопровождающих движение транспорта, у которого отсутствует катализатор.
Чаще всего просто удаляют катализатор, а на его место устанавливают пламегаситель, который выравнивает поток выхлопных газов. Его рекомендуется использовать для устранения неприятных шумов, сопровождающих движение транспорта, у которого отсутствует катализатор.
Если было решено удалить катализатор, то рекомендуется его полностью снять, а не прибегать к рекомендации автомобилистов просто пробить отверстие в нем. Такая процедура способна слегка улучшить ситуацию на некоторое время.
В машине, которая соответствует экологическому стандарту Евро-3, требуется не только удалить катализатор, но и выполнить перепрошивку ЭБУ. Обновление выполняется до версии, в которой каталитический нейтрализатор отсутствует.
Дополнительно можно установить эмулятор сигнала от кислородного датчика, чтобы не потребовалось перепрошивать ЭБУ полностью.
Самое лучшее решение при поломке каталитического нейтрализатора – это его замена на оригинальный компонент в рамках специализированного сервиса, где работают профессиональные мастера с достаточным опытом. Это обеспечивает исключение вмешательства в конструкцию автомобиля, поэтому сохранится соответствие его экологического класса стандарту, прописанному производителем.
Это обеспечивает исключение вмешательства в конструкцию автомобиля, поэтому сохранится соответствие его экологического класса стандарту, прописанному производителем.
Самостоятельная диагностика работы катализатора
Если машина стала ездить хуже, а на приборной панели загорелся «чек», то можно отправиться в сервисный центр, где после тщательной диагностики станет понятно, что произошло. Однако можно самостоятельно выполнить элементарную диагностику функционирования катализатора:
- Оценить оттенок выхлопа: если он черный, то это явный признак того, что нейтрализатор не работает, поэтому через него и проходят все вредные вещества и газу наружу.
- Оценить давление газов, выходящих наружу: если приложить ладонь к отверстию выхлопной трубы, то напор должен быть высоким. Если он низкий, то это свидетельствует о необходимости замены катализатора.
- После длительной поездки заглянуть под машину: если корпус катализатора раскален, то можно говорить о снижении его пропускной способности.

- В сервисе можно проверить давление выхлопа и сравнить его с показателями эталонных данных. Для определения давления манометр размещается там, где обычно установлен лямбда-зонд.
- Визуально можно оценить демонтированный нейтрализатор выхлопа на предмет оплавления, засорения или выгорания.
Заменить катализатор требуется после того, как точно установлено, что проблемы в работе автомобиля возникли из-за оплавленных или забитых сот. Но рекомендуется отыскать причину, по которой случилось засорение нейтрализатора, так как после установке нового элемента он тоже может пострадать от тех же неполадок. Поэтому в современных авто все системы связаны очень сильно, для чего используется большое количество датчиков.
Как работает катализатор
Миллионы машин в мире – источники загрязнения окружающей среды. Особенно плохо обстоят дела в больших городах, где вредные выхлопы представляют реальную угрозу для жителей.
Расположение катализатора в современных машинах.

Миллионы машин в мире – источники загрязнения окружающей среды. Особенно плохо обстоят дела в больших городах, где вредные выхлопы представляют реальную угрозу для жителей.
Чтобы решать эту проблему, правительства стран принимают законы, устанавливающие пределы выброса вредных веществ, в которые должны вписываться эксплуатируемые машины. Для соответствия этим законам производители автомобилей постоянно работают над двигателями и топливными системами. Для дальнейшего уменьшения вредных выбросов были изобретены катализаторы, которые входят в контакт с отработавшими газами и сильно уменьшают вредные выхлопы.
В этой статье Вы познакомитесь, какие вредные вещества производит двигатель, и как катализатор борется с каждым из них. Катализаторы – удивительно простые устройства, поэтому Вам будет интересно узнать, насколько эффективно они работают!
Вредные выхлопы автомобиля
Для уменьшения вредных выхлопов современные машины тщательно контролируют количество сгораемого топлива. Для этого соотношение топлива и воздуха поддерживается на близком к стехиометрическому уровне, то есть на идеальном расчетном уровне. Теоретически это соотношение означает, что происходит сгорание всего топлива и кислорода воздуха. Для бензина стехиометрическое соотношение — 14.7:1. Топливная смесь лишь немного отклоняется от этого идеального соотношения во время езды. Иногда смесь бывает бедной (соотношение воздух-топливо больше 14.7) или богатой (соотношение воздух-топливо меньше 14.7).
Для этого соотношение топлива и воздуха поддерживается на близком к стехиометрическому уровне, то есть на идеальном расчетном уровне. Теоретически это соотношение означает, что происходит сгорание всего топлива и кислорода воздуха. Для бензина стехиометрическое соотношение — 14.7:1. Топливная смесь лишь немного отклоняется от этого идеального соотношения во время езды. Иногда смесь бывает бедной (соотношение воздух-топливо больше 14.7) или богатой (соотношение воздух-топливо меньше 14.7).
Главные составляющие выхлопа автомобиля:
Азот (N2) – воздух на 78% состоит из азота, и большая часть его проходит через двигатель.
Оксид углерода (CO2) – это один из продуктов работы двигателя. Углерод в топливе связывается с кислородом в воздухе.
Пары воды (h3O) – еще один продукт сгорания. Водород в топливе связывается с кислородом в воздухе.
Эти части выхлопа практически безобидные (хотя оксид углерода вносит вклад в глобальное потепление). Но процесс сгорания не бывает идеальным и приводит к малым выбросам более вредных и опасных газов:
Окись углерода (CO) или угарный газ – ядовитый газ без цвета и запаха.
Гидрокарбонаты и летучие органические вещества (VOC) – получаются из-за не прогоревшего полностью топлива
Солнечный свет разрушает эти соединения, и получаются окиси — продукты фотохимического разложения выхлопных газов, которые входят в реакцию с оксидом азота и образуют слой озона (O3), главного компонента смога.
Окись азота (NO и NO2, называемые вместе NOx) – вносят вклад в смог и кислотные дожди, а также вызывают раздражения слизистой человека.
Три выше упомянутые вредные составляющие выхлопа должны уменьшаться в количестве при прохождении через катализатор.
Большинство современных машин оснащено трехкомпонентными катализаторами.
«Три компонента» относятся к трем вредным выхлопам, которые надо нейтрализовать – угарный газ СО, углеводороды VOC и окись NOx. Именно благодаря трем компонентам происходят необходимые химические реакции – окисление монооксида углерода (СО) и несгоревших углеводородов (СН), а также сокращение количества окиси азота (NOx). В трехкомпонентном катализаторе платина и палладий вызывают окисление СО и СН, а родий уменьшает выбросы NOx. Катализатор представляет сотовую структуру из керамики. Это позволяет максимально увеличить эффективную площадь контакта каталитического покрытия с выхлопными газами — до величин около 20 тыс. м2. Причем вес благородных металлов, нанесенных на подложку на этой огромной площади, составляет всего 2-3 грамма! Керамика сделана достаточно огнеупорной – выдерживает температуру до 800-850 градусов. Но все равно при неисправности системы питания и длительной работе на богатой рабочей смеси монолит может не выдержать и оплавиться — и тогда катализатор выйдет из строя. Именно поэтому так проблематично выглядит использование катализаторов с керамическим носителем на карбюраторных двигателях.
В трехкомпонентном катализаторе платина и палладий вызывают окисление СО и СН, а родий уменьшает выбросы NOx. Катализатор представляет сотовую структуру из керамики. Это позволяет максимально увеличить эффективную площадь контакта каталитического покрытия с выхлопными газами — до величин около 20 тыс. м2. Причем вес благородных металлов, нанесенных на подложку на этой огромной площади, составляет всего 2-3 грамма! Керамика сделана достаточно огнеупорной – выдерживает температуру до 800-850 градусов. Но все равно при неисправности системы питания и длительной работе на богатой рабочей смеси монолит может не выдержать и оплавиться — и тогда катализатор выйдет из строя. Именно поэтому так проблематично выглядит использование катализаторов с керамическим носителем на карбюраторных двигателях.
Трехкомпонентный каталитический нейтрализатор
А- катализатор уменьшения вредных выхлопов, В- катализатор окисления (сгорания) вредных веществ, С- керамическая сотовая структура
Обратите внимание на две раздельные части катализаторов
Большинство катализаторов используют сотовую структуру.
Керамическая сотовая структура катализатора
Первая часть катализатора использует платину и родий для уменьшения выхлопа NOx. При контакте с молекулами NO или NO2 катализатор отрываем азот N из соединения, тем самым, освобождая азот O2. Атомы азота образуют соединение азота N2. Формула процесса:
2NO => N2 + O2 или 2NO2 => N2 + 2O2
Окисляющий катализатор – второй этап очистки.
Он уменьшает выбросы несгоревших углеводородов и моноксида углерода путем сжигания их (окислением) в платиновом и палладиевом катализаторе. Этот катализатор ускоряет реакцию CO и углеводородов с несгоревшим кислородом в выхлопном газе. Формула:
2CO + O2 => 2CO2
Но откуда берется этот кислород?
Контрольная система – это третий этап. Она контролирует состав выходящих газов и использует эту информацию для контроля впрыска. Перед катализатором установлен кислородный датчик или лямбда-зонд. Этот датчик сообщает блоку управления двигателем, сколько кислорода в выхлопном газе. Сам блок управления может увеличивать или уменьшать количество кислорода в топливной смеси. Эта контрольная схема позволяет компьютеру устанавливать близкое к стехиометрическому соотношение топлива к воздуха, а так же обеспечивать достаточное количество кислорода в выхлопе, чтобы окислялись гидрокарбонаты и CO.
Сам блок управления может увеличивать или уменьшать количество кислорода в топливной смеси. Эта контрольная схема позволяет компьютеру устанавливать близкое к стехиометрическому соотношение топлива к воздуха, а так же обеспечивать достаточное количество кислорода в выхлопе, чтобы окислялись гидрокарбонаты и CO.
Другие способы уменьшения вредных выхлопов.
Катализатор существенно уменьшает вредные выхлопы автомобиля, но его можно еще дальше совершенствовать. Большой недостаток катализатора – высокий температурный режим работы. Когда Вы запускаете холодный автомобиль, сначала катализатор вообще не работает, и все вредные выбросы выходят в окружающую среду.
Простое решение этой проблемы – разместить катализатор ближе к двигателю. Это позволит ему прогреваться быстрее, но также уменьшает срок эксплуатации из-за работы при повышенных температурах. Большинство производителей размещают катализатор под передним пассажирским сиденьем, чтобы увеличить срок службы устройства.
Предварительный прогрев катализатора – хороший способ вывести его раньше на рабочий температурный режим. Самый простой способ –электрический нагревательный элемент. К сожалению, 12 Вольт автомобильной сети недостаточно для быстрого прогрева катализатора. Кроме того, большинство водителей не будут ждать несколько минут на прогрев катализатора до запуска машины. Сегодня только гибридные машины располагают достаточным напряжением для быстрого прогрева катализатора.
DOE объясняет…Катализаторы | Министерство энергетики
Офис
Наука
Реальный катализатор (фоновое изображение) и схема каталитического этапа (переднее изображение). Реагирующие молекулы (слева) приобретают энергию, чтобы преодолевать энергетический барьер и превращаться в молекулы продукта (справа).
Изображение предоставлено Аргоннской национальной лабораторией
Катализатор — это вещество, которое ускоряет химическую реакцию или снижает температуру или давление, необходимые для ее запуска, при этом само не расходуется во время реакции. Катализ — это процесс добавления катализатора для облегчения реакции.
Катализ — это процесс добавления катализатора для облегчения реакции.
Во время химической реакции связи между атомами в молекулах разрываются, перестраиваются и перестраиваются, рекомбинируя атомы в новые молекулы. Катализаторы делают этот процесс более эффективным, снижая энергию активации , которая представляет собой энергетический барьер, который необходимо преодолеть, чтобы произошла химическая реакция. В результате катализаторы облегчают разрыв атомов и образование химических связей для образования новых комбинаций и новых веществ.
Использование катализаторов приводит к более быстрым и энергоэффективным химическим реакциям. Катализаторы также обладают ключевым свойством, называемым селективностью , с помощью которого они могут направлять реакцию для увеличения количества желаемого продукта и уменьшения количества нежелательных побочных продуктов. Они могут производить совершенно новые материалы с совершенно новыми потенциальными применениями.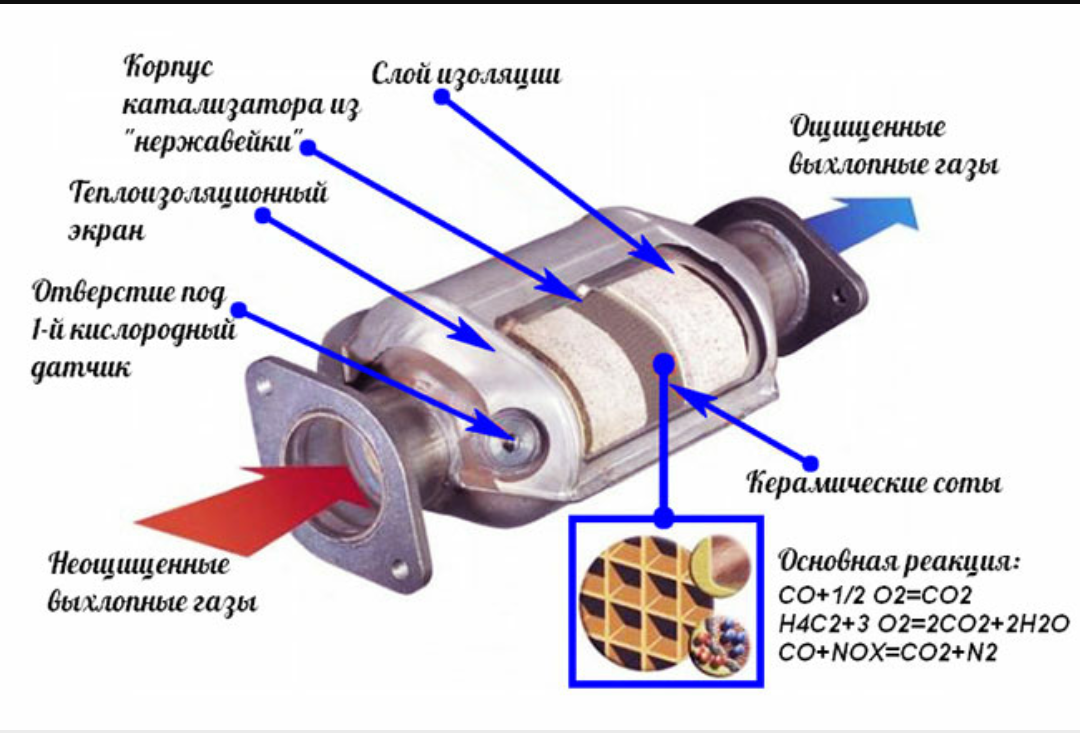
За последние несколько десятилетий ученые разрабатывали все более специализированные катализаторы для важных реальных приложений. В частности, мощные катализаторы изменили химическую промышленность. Эти достижения привели к созданию биоразлагаемых пластиков, новых фармацевтических препаратов и экологически безопасных видов топлива и удобрений.
Департамент науки Министерства энергетики США: вклад в исследование катализаторов
Программа фундаментальных энергетических наук Департамента энергетики (DOE) активно поддерживает фундаментальные исследования катализаторов. Министерство энергетики занимается разработкой новых катализаторов и использованием катализаторов для контроля химических превращений на молекулярном и субмолекулярном уровнях. В исследованиях Министерства энергетики особое внимание уделяется пониманию этих реакций и тому, как сделать их более эффективными и целенаправленными. Главной целью Министерства энергетики является разработка новых концепций катализа и новых катализаторов, которые помогут промышленности более эффективно и устойчиво производить топливо и химикаты из ископаемого и возобновляемого сырья. Это исследование помогает продвигать солнечное топливо, которое компании производят, используя солнце и обычные химические вещества, такие как углекислый газ и азот. Это исследование также создает передовые методы преобразования выброшенного пластика в новые продукты.
Это исследование помогает продвигать солнечное топливо, которое компании производят, используя солнце и обычные химические вещества, такие как углекислый газ и азот. Это исследование также создает передовые методы преобразования выброшенного пластика в новые продукты.
Краткие факты
- Люди используют катализаторы тысячи лет. Например, дрожжи, которые мы используем для приготовления хлеба, содержат ферменты, которые являются природными катализаторами, способствующими превращению муки в хлеб.
- Нобелевская премия по химии 2005 г. была присуждена трем исследователям (Иву Шовену, Роберту Х. Граббсу и Ричарду Р. Шроку) за работу над катализаторами метатезиса. доктора Граббс и Шрок частично финансировались Министерством энергетики за свои исследования, получившие Нобелевскую премию. Доктор Шрок продолжает финансироваться Министерством энергетики.
- Нобелевская премия по химии 2018 года была присуждена Фрэнсис Х. Арнольд за ее новаторскую работу по управлению эволюцией ферментов для таких приложений, как возобновляемые виды топлива, безвредные для окружающей среды.
 Она частично финансируется Министерством энергетики.
Она частично финансируется Министерством энергетики. - Посетите Аргоннскую национальную лабораторию, чтобы узнать еще о семи вещах, которые вы, возможно, не знали о катализе.
Ресурсы
- Программа BES Управления науки Министерства энергетики США
- Узнайте о направлениях исследований Министерства энергетики США в области химических катализаторов.
- Отчет: Потребности в фундаментальных исследованиях для науки о катализе
- Как катализаторы меняют химическую промышленность, солнечное топливо и переработку полимеров.
- Научные достижения: катализ видит свет
- Научное достижение: ученые наблюдают, как свет разрушает модельный фотокатализатор в режиме, близком к реальному времени
Научные термины могут сбивать с толку. Объяснения DOE предлагают простые объяснения ключевых слов и понятий в фундаментальной науке. В нем также описывается, как эти концепции применяются к работе, которую проводит Управление науки Министерства энергетики, помогая Соединенным Штатам преуспеть в исследованиях по всему научному спектру.
Катализаторы и энергия активации | ChemTalk
Что такое катализатор?
Поговорим о том, что такое катализаторы. Катализатор представляет собой соединение или элемент, который увеличивает скорость химической реакции, например. скорость, с которой это происходит, не будучи частью реакции. Вообще говоря, катализатор не разрушается, не расходуется и не изменяется навсегда в ходе реакции. Катализатор делает это, понижая энергия активации , которую мы объясним в следующем разделе.
Катализаторы работают, предоставляя альтернативный путь реакции, который имеет более низкую энергию активации, что облегчает реагентам образование продуктов. Это позволяет реакции происходить быстрее и эффективнее. Катализаторы могут быть как природными, так и синтетическими, и они обычно используются в промышленности, чтобы сделать химические реакции более эффективными и экономичными.
Например, ферменты — это природные катализаторы, необходимые для многих химических реакций, протекающих в нашем организме, а промышленные катализаторы используются в производстве широкого спектра продуктов, включая пластмассы, топливо и фармацевтические препараты.
Что такое энергия активации?
Проще говоря, энергия активации определяется как энергия, необходимая для начала реакции между двумя или более элементами или соединениями. Реакция с высокой энергией активации может протекать медленно или вообще не идти. Чтобы ускорить или начать реакцию, вы можете либо добавить необходимую энергию активации, либо использовать катализатор, который снижает это требование, эффективно ускоряя реакцию.
Единицы энергии активации выражены в единицах энергии. Наиболее распространенными единицами измерения являются кДж/моль или Дж/моль.
Как работает катализатор?
Катализатор увеличивает скорость реакции за счет снижения энергии активации. Пониженная энергия активации означает, что для начала реакции требуется меньше энергии.
Пониженная энергия активации означает, что для начала реакции требуется меньше энергии.
На приведенном ниже графике показана энергия реакции как с катализатором, так и без него. Ось x представляет собой координату реакции или развитие реакции от реагента (слева) к продукту (справа). Ось Y — это энергия.
Энергия реакции с катализатором и без него. (Источник: Wikipedia Commons)
При наличии катализатора энергия активации (E a ) меньше. Визуально, холм, на который должна подняться реакция, прежде чем спуститься вниз к продуктам, меньше. Точно так же, как ехать на велосипеде по небольшому подъему легче, чем по большому, реакция протекает быстрее, когда холм с энергией активации меньше.
Катализатор снижает энергию активации, изменяя переходное состояние реакции. Затем реакция идет по другому пути/механизму, чем некатализируемая реакция. Катализатор не изменяет чистую разницу энергии между реагентом и продуктом. Итоговое уравнение реакции будет одинаковым для катализируемой и некатализируемой реакции, даже если изменится переходное состояние.
Общая реакция: A + B + катализатор -> AB + катализатор
Чистая реакция: A + B -> AB
Основные категории катализатора s
Гетерогенные катализаторы другая фаза, чем реагенты. Обычно это означает, что катализатор находится в твердой фазе, а реагенты находятся в жидкой или газовой фазе. Другое название гетерогенного катализатора — поверхностный катализатор.
Гетерогенные катализаторы работают, прикрепляя катализатор к твердой несущей структуре, и реагенты протекают над катализатором и мимо него, реагируя по пути. Преимущество этого типа катализатора заключается в том, что катализатор легко отделяется от продукта после завершения реакции. После этого катализатор можно легко использовать повторно. В производстве это важная мера снижения затрат. Недостатком гетерогенного катализатора является то, что степень взаимодействия между реагентом и катализатором может быть ограничена площадью поверхности и диффузией продукта от поверхности.
Распространенным гетерогенным катализатором является каталитический нейтрализатор бензина в автомобилях. Другим важным гетерогенным катализатором является процесс Габера-Боша, в результате которого образуется NH 3 .
Гомогенные катализаторы
В гомогенном катализаторе и реагенты, и катализатор находятся в одной фазе. Обычно они оба находятся либо в жидкой, либо в газовой фазе.
Основным преимуществом гомогенного катализатора является усиление взаимодействия между реагентом и катализатором. Оба могут свободно двигаться и, следовательно, с большей вероятностью будут взаимодействовать и приводить к реакции.
Обычными гомогенными катализаторами являются переходные металлы и кислоты. Одной из гомогенных катализируемых реакций является превращение кислорода в озон в атмосфере. Оксид азота (NO) катализирует реакцию. Все участники реакции находятся в газовой фазе. Следовательно, мы знаем, что это гомогенная каталитическая реакция.
Ферменты
Ферменты представляют собой крупные белки, являющиеся биологическими катализаторами. Они являются мощными силами в теле. Часто они катализируют только одну очень специфическую реакцию (по сравнению с неорганическими катализаторами, которые часто катализируют гораздо более широкий набор реакций). Специфичность обусловлена активным центром в катализаторе — карманом определенного химического состава, образованным аминокислотами, куда подходит только одна очень конкретная модель реагента. Это также называется моделью замка и ключа.
Они являются мощными силами в теле. Часто они катализируют только одну очень специфическую реакцию (по сравнению с неорганическими катализаторами, которые часто катализируют гораздо более широкий набор реакций). Специфичность обусловлена активным центром в катализаторе — карманом определенного химического состава, образованным аминокислотами, куда подходит только одна очень конкретная модель реагента. Это также называется моделью замка и ключа.
Ферменты играют важную роль в организме. Они катализируют расщепление крахмала с образованием глюкозы. Они также преобразуют углекислый газ (CO 2 ) в другие молекулы, необходимые организму, такие как HCO 3 – . Ферменты помогают и ускоряют почти все процессы в организме.
Расчет энергии активации
Для расчета энергии активации используется уравнение Аррениуса. Здесь мы рассмотрим основы, но для получения дополнительных примеров и углубленного анализа обязательно ознакомьтесь со статьей об уравнении Аррениуса.
Уравнение Аррениуса:
Где – константа скорости, – энергия активации, – коэффициент частоты, – газовая постоянная, – температура.
Мы можем найти энергию активации, если знаем константу скорости () при различных температурах (). Чтобы определить энергию активации (), мы строим график зависимости от . Таким образом, мы получаем линию с наклоном –/ и точкой пересечения с осью y. является константой, поэтому мы можем найти энергию активации.
Например, задачи на формулу энергии активации см. на странице уравнения Аррениуса!
Список распространенных катализаторов:
- Пентоксид ванадия (для получения серной кислоты)
- Металлический палладий
- Диоксид марганца
- Металлическая платина (в каталитических нейтрализаторах)
- Металлическое железо (в процесс)
- Хлорид алюминия (многие органические реакции)
- Оксид меди (II)
- Ферменты (природные катализаторы в биохимических реакциях)
Катализаторы и энергия активации Словарь определений
- Энергия активации — Энергия, необходимая для запуска реакции между двумя или более элементами или соединениями
- Катализатор — молекула, которая увеличивает скорость реакции и не потребляется в реакции
- Оборот — число.



 Металл не способен образовывать мелкие частицы, поэтому для двигателя он не представляет опасности.
Металл не способен образовывать мелкие частицы, поэтому для двигателя он не представляет опасности.
 Она частично финансируется Министерством энергетики.
Она частично финансируется Министерством энергетики.