Как составить электронную формулу химического элемента в неорганической химии. Марганец электронно графическая формула
Электронная и электронно-графическая формула в химии
Что такое электронная и электронно-графическая формула
Наиболее часто электронные формулы записывают для атомов в основном или возбужденном состоянии и для ионов.
Существует несколько правил, которые необходимо учитывать при составлении электронной формулы атома химического элемента. Это принцип Паули, правила Клечковского или правило Хунда.
Составление электронной и электронно-графической формулы
При составление электронной формулы следует учитывать, что номер периода химического элемента определяет число энергетических уровней (оболочек) в атоме, а его порядковый номер количество электронов.
Согласно правилу Клечковского, заполнение энергетических уровней происходит в порядке возрастания суммы главного и орбитального квантовых чисел (n + l), а при равных значениях этой суммы – в порядке возрастания n:
1s < 2s < 2p < 3s < 3p < 4s ≈ 3d < 4p < 5s ≈ 4d < 5p < 6s ≈ 5d ≈ 4f < 6p и т.д.
Так, значению n + l = 5 соответствуют энергетические подуровни 3d (n = 3, l=2), 4d (n=4, l=1) и 5s (n=5, l =0). Первым из этих подуровней заполняется тот, у которого ниже значение главного квантового числа.
Поведение электронов в атомах подчиняется принципу запрета, сформулированному швейцарским ученым В. Паули: в атоме не может быть двух электронов, у которых были бы одинаковыми все четыре квантовых числа. Согласно принципу Паули, на одной орбитали, характеризуемой определенными значениями трех квантовых чисел (главное, орбитальное и магнитное), могут находиться только два электрона, отличающиеся значением спинового квантового числа. Из принципа Паули вытекает следствие: максимально возможное число электронов на каждом энергетическом уровне равно удвоенному значению квадрата главного квантового числа.
Электронную формулу атома изображают следующим образом: каждому энергетическому уровню соответствует определенное главное квантовое число n, обозначаемое арабской цифрой; за каждой цифрой следует буква, соответствующая энергетическому подуровню и обозначающая орбитальное квантовое число. Верхний индекс у буквы показывает число электронов, находящихся в подуровне. Например, электронная формула атома натрия имеет следующий вид:
11N 1s22s22p63s1.
При заполнение электронами энергетических подуровней также необходимо соблюдать правило Хунда: в данном подуровне электроны стремятся занять энергетические состояния таким образом, чтобы суммарный спин был максимальным, что наиболее наглядно отражается при составлении электронно-графических формул.
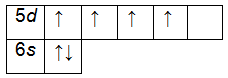
Электронно-графические формулы обычно изображают для валентных электронов. В такой формуле все электроны помечаются стрелочками, а ячейками (квадратиками) – орбитали. В одной ячейке не может находиться более двух электронов. Рассмотрим на примере ванадия. Сначала записываем электронную формулу и определяем валентные электроны:
+74 W)2)8)18)32)12)2;
1s22s22p63s23p63d104s24p64f145s25p65d46s2.
Внешний энергетический уровень атома вольфрама содержит 6 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
Примеры решения задач
ru.solverbook.com
Как составить электронную формулу химического элемента в неорганической химии :: SYL.ru
Выясним, как составить электронную формулу химического элемента. Этот вопрос является важным и актуальным, так как дает представление не только о строении, но и о предполагаемых физических и химических свойствах рассматриваемого атома.
Правила составления
Для того чтобы составить графическую и электронную формулу химического элемента, необходимо иметь представление о теории строения атома. Начнем с того, что есть два основных компонента атома: ядро и отрицательные электроны. Ядро включает в себя нейтроны, которые не имеют заряда, а также протоны, обладающие положительным зарядом.
Рассуждая, как составить и определить электронную формулу химического элемента, отметим, что для нахождения числа протонов в ядре, потребуется периодическая система Менделеева.
Номер элемента по порядку соответствует количеству протонов, находящихся в его ядре. Номер периода, в котором располагается атом, характеризует число энергетических слоев, располагаются на которых электроны.
Для определения количества нейтронов, лишенных электрического заряда, необходимо из величины относительной массы атома элемента, отнять его порядковый номер (количество протонов).
Инструкция
Для того чтобы понять, как составить электронную формулу химического элемента, рассмотрим правило заполнения отрицательными частицами подуровней, сформулированное Клечковским.
В зависимости от того, каким запасом свободной энергии обладают свободные орбитали, составляется ряд, характеризующий последовательность заполнения уровней электронами.
Каждая орбиталь содержит всего два электрона, которые располагаются антипараллельными спинами.
Для того чтобы выразить структуру электронных оболочек, применяют графические формулы. Как выглядят электронные формулы атомов химических элементов? Как составлять графические варианты? Эти вопросы включены в школьный курс химии, поэтому остановимся на них подробнее.
Существует определенная матрица (основа), которую используют при составлении графических формул. Для s-орбитали характерна только одна квантовая ячейка, в которой противоположно друг другу располагается два электрона. Их в графическом виде обозначаются стрелками. Для р-орбитали изображают три ячейки, в каждой также находится по два электрона, на d орбитали располагается десять электронов, а f заполняется четырнадцатью электронами.
Примеры составления электронных формул
Продолжим разговор о том, как составить электронную формулу химического элемента. Например, нужно составить графическую и электронную формулу для элемента марганца. Сначала определим положение данного элемента в периодической системе. Он имеет 25 порядковый номер, следовательно, в атоме располагается 25 электронов. Марганец - это элемент четвертого периода, следовательно, у него четыре энергетических уровня.
Как составить электронную формулу химического элемента? Записываем знак элемента, а также его порядковый номер. Пользуясь правилом Клечковского, распределяем по энергетическим уровням и подуровням электроны. Последовательно располагаем их на первом, втором, а также третьем уровне, вписывая в каждую ячейку по два электрона.
Далее суммируем их, получая 20 штук. Три уровня в полном объеме заполнены электронами, а на четвертом остается только пять электронов. Учитывая, что для каждого вида орбитали характерен свой запас энергии, оставшиеся электроны распределяем на 4s и 3d подуровень. В итоге готовая электронно-графическая формула для атома марганца имеет следующий вид:
1s2 / 2s2, 2p6 / 3s2, 3p6 / 4s2, 3d3
Практическое значение
С помощью электронно-графических формул можно наглядно увидеть число свободных (неспаренных) электронов, определяющих валентность данного химического элемента.
Предлагаем обобщенный алгоритм действий, с помощью которого можно составить электронно-графические формулы любых атомов, располагающихся в таблице Менделеева.
В первую очередь необходимо определить количество электронов, используя периодическую систему. Цифра периода указывает на численность энергетических уровней.
Принадлежность к определенной группе связана с количеством электронов, находящихся на наружном энергетическом уровне. Подразделяют уровни на подуровни, заполняют их с учетом правила Клечковского.
Заключение
Для того чтобы определить валентные возможности любого химического элемента, расположенного в таблице Менделеева, необходимо составить электронно-графическую формулу его атома. Алгоритм, приведенный выше, позволит справиться с поставленной задачей, определить возможные химические и физические свойства атома.
www.syl.ru
Как написать электронно-графическую формулу | Сделай все сам
Дабы обучиться составлять электронно-графические формулы, значимо осознать теорию строения ядерного ядра. Ядро атома составляют протоны и нейтроны. Вокруг ядра атома на электронных орбиталях находятся электроны.
Вам понадобится
- — ручка;
- — бумага для записей;
- — периодическая система элементов (таблица Менделеева).
Инструкция
1. Электроны в атоме занимают свободные орбитали в последовательности, называемой шкалой энергии:1s / 2s, 2p / 3s, 3p / 4s, 3d, 4p / 5s, 4d, 5p / 6s, 4d, 5d, 6p / 7s, 5f, 6d, 7p. На одной орбитали могут располагаться два электрона с противоположными спинами – направлениями вращения.
2. Конструкцию электронных оболочек выражают с поддержкой графических электронных формул. Для записи формулы используйте матрицу. В одной ячейке могут располагаться один либо два электрона с противоположными спинами. Электроны изображаются стрелками. Матрица наглядно показывает, что на s-орбитали могут располагаться два электрона, на p-орбитали – 6, на d – 10, на f -14.
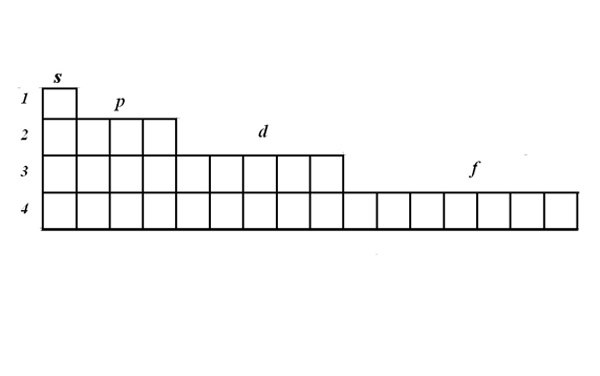
3. Разглядите правило составления электронно-графической формулы на примере марганца. Обнаружьте марганец в таблице Менделеева. Его порядковый номер 25, значит в атоме 25 электронов, это элемент четвертого периода.
4. Запишите порядковый номер и символ элемента рядом с матрицей. В соответствии со шкалой энергии заполоните ступенчато 1s, 2s, 2p, 3s, 3p, 4s ярусы, вписав по два электрона в ячейку. Получится 2+2+6+2+6+2=20 электронов. Эти ярусы заполнены всецело.
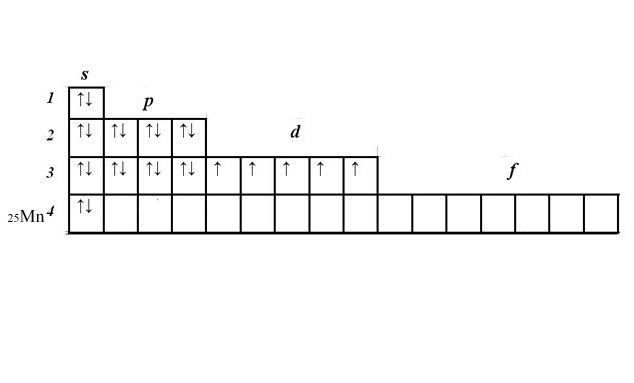
5. У вас осталось еще пять электронов и незаполненный 3d-ярус. Расположите электроны в ячейках d-подуровня, начиная слева. Электроны с идентичными спинами расположите в ячейках вначале по одному. Если все ячейки заполнены, начиная слева, добавьте по второму электрону с противоположным спином. У марганца пять d-электронов, расположенных по одному в всей ячейке.
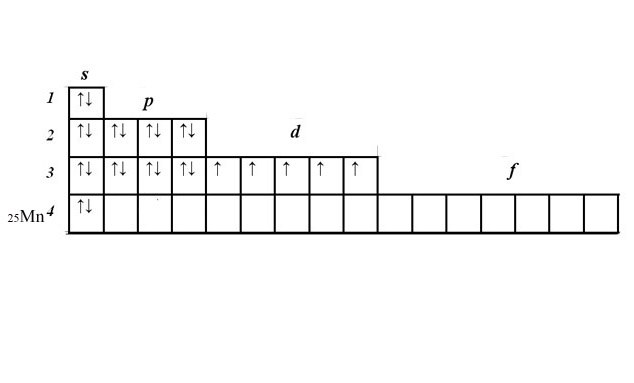
6. Электронно-графические формулы наглядно показывают число неспаренных электронов, которые определяют валентность.
При создании теоретических и фактических работ по математике, физике, химии студент либо школьник сталкивается с необходимостью вставки особых символов и трудных формул. Располагая приложением Word из офисного пакета Microsoft, дозволено набрать электронную формулу всякий трудности.
Инструкция
1. Откройте новейший документ в Microsoft Word. Присвойте ему наименование и сбережете в той же папке, где у вас лежит работа, дабы в грядущем не искать.
2. Перейдите на вкладку «Вставка». Справа обнаружьте символ ?, а рядом надпись «Формула». Нажмите на стрелочку. Появится окно, в котором вы можете предпочесть встроенную формулу, скажем, формулу квадратного уравнения.
3. Нажмите на стрелку и на верхней панели появятся самые различные символы, которые вам могут потребоваться при написании определенно этой формулы. Изменив ее так, как надобно вам, вы можете сберечь ее. С этого момента она будет выпадать в списке встроенных формул.
4. Если вам необходимо перенести формулу в текст, тот, что позднее надобно поместить на сайте, то кликните на энергичном поле с ней правой кнопкой мыши и выберите не высокопрофессиональный, а линейный метод написания. В частности, формула все того же квадратного уравнения в данном случае примет вид:x=(-b±?(b^2-4ac))/2a.
5. Иной вариант написания электронной формулы в Word – через конструктор. Зажмите единовременно клавиши Alt и =. У вас сразу появится поле для написания формулы, а в верхней панели откроется конструктор. Тут вы можете предпочесть все знаки, которые могут потребоваться для записи уравнения и решения всякий задачи.
6. Некоторые символы линейной записи могут быть неясными читателю, неизвестному с компьютерной символикой. В этом случае самые трудные формулы либо уравнения имеет толк сберечь в графическом виде. Для этого откройте самый легкой графический редактор Paint: «Пуск» — «Программы» — «Paint». После этого увеличьте масштаб документа с формулой так, дабы она заняла каждый экран. Это нужно, дабы сохраненное изображение имело наибольшее разрешение. Нажмите на клавиатуре PrtScr, перейдите в Paint и нажмите Ctrl+V.
7. Обрежьте все лишнее. В результате у вас получится добротное изображение с необходимой формулой.
Видео по теме
Обратите внимание! Помните, что химия – наука исключений. У атомов побочных подгрупп Периодической системы встречается «проскок» электрона. Скажем, у хрома с порядковым номером 24 один из электронов с 4s-яруса переходит в ячейку d-яруса. Схожий результат есть у молибдена, ниобия и др. Помимо того, есть представление возбужденного состояния атома, когда спаренные электроны распариваются и переходят на соседние орбитали. Следственно при составлении электронно-графических формул элементов пятого и последующих периодов побочной подгруппы сверяйтесь со справочником.
jprosto.ru
Электронные формулы атомов химических элементов
Электронные формулы атомов химических элементов, слои расположены в порядке заполнения подуровней. Электронные слои атомов заполняются электронами в порядке, согласно правилу Клечковского.
Порядок заполнения атомных орбиталей по мере увеличения энергии следующий: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f ≈ 5d < 6p < 7s < 5f ≈ 6d < 7p < 8s. При заполнении орбитальных оболочек атома более предпочтительны (более энергетически выгодны), и, значит, заполняются раньше те состояния, для которых сумма главного квантового числа n и побочного (орбитального) квантового числа l , т.е. n + l , имеет меньшее значение.
| s-элементы | d-элементы | f-элементы | p-элементы |
| № | Знак | Элемент | Электронная формула |
| I период | |||
| 1 | H | водород | 1s1 |
| 2 | He | гелий | 1s2 |
| № | Знак | Элемент | Электронная формула |
| II период | |||
| 3 | Li | литий | 1s2 2s1 |
| 4 | Be | бериллий | 1s2 2s2 |
| 5 | B | бор | 1s2 2s2 2p1 |
| 6 | C | углерод | 1s2 2s2 2p2 |
| 7 | N | азот | 1s2 2s2 2p3 |
| 8 | O | кислород | 1s2 2s2 2p4 |
| 9 | F | фтор | 1s2 2s2 2p5 |
| 10 | Ne | неон | 1s2 2s2 2p6 |
| № | Знак | Элемент | Электронная формула |
| III период | |||
| 11 | Na | натрий | 1s2 2s2 2p6 3s1 |
| 12 | Mg | магний | 1s2 2s2 2p6 3s2 |
| 13 | Al | алюминий | 1s2 2s2 2p6 3s2 3p1 |
| 14 | Si | кремний | 1s2 2s2 2p6 3s2 3p2 |
| 15 | P | фосфор | 1s2 2s2 2p6 3s2 3p3 |
| 16 | S | сера | 1s2 2s2 2p6 3s2 3p4 |
| 17 | Cl | хлор | 1s2 2s2 2p6 3s2 3p5 |
| 18 | Ar | аргон | 1s2 2s2 2p6 3s2 3p6 |
| № | Знак | Элемент | Электронная формула |
| IV период | |||
| 19 | K | калий | 1s2 2s2 2p6 3s2 3p6 4s1 |
| 20 | Ca | кальций | 1s2 2s2 2p6 3s2 3p6 4s2 |
| 21 | Sc | скандий | 1s2 2s2 2p6 3s2 3p6 4s2 3d1 |
| 22 | Ti | титан | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 |
| 23 | V | ванадий | 1s2 2s2 2p6 3s2 3p6 4s2 3d3 |
| 24 | Cr | хром | 1s2 2s2 2p6 3s2 3p6 4s1 3d5 |
| 25 | Mn | марганец | 1s2 2s2 2p6 3s2 3p6 4s2 3d5 |
| 26 | Fe | железо | 1s2 2s2 2p6 3s2 3p6 4s2 3d6 |
| 27 | Co | кобальт | 1s2 2s2 2p6 3s2 3p6 4s2 3d7 |
| 28 | Ni | никель | 1s2 2s2 2p6 3s2 3p6 4s2 3d8 |
| 29 | Cu | медь | 1s2 2s2 2p6 3s2 3p6 4s1 3d10 |
| 30 | Zn | цинк | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 |
| 31 | Ga | галлий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p1 |
| 32 | Ge | германий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p2 |
| 33 | As | мышьяк | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3 |
| 34 | Se | селен | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4 |
| 35 | Br | бром | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 |
| 36 | Kr | криптон | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 |
| № | Знак | Элемент | Электронная формула |
| V период | |||
| 37 | Rb | рубидий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 |
| 38 | Sr | стронций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 |
| 39 | Y | иттрий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1 |
| 40 | Zr | цирконий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d2 |
| 41 | Nb | ниобий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d4 |
| 42 | Mo | молибден | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d5 |
| 43 | Tc | технеций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d5 |
| 44 | Ru | рутений | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d7 |
| 45 | Rh | родий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d8 |
| 46 | Pd | палладий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s0 4d10 |
| 47 | Ag | серебро | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10 |
| 48 | Cd | кадмий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 |
| 49 | In | индий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1 |
| 50 | Sn | олово | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p2 |
| 51 | Sb | сурьма | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s22 4d10 5p3 |
| 52 | Te | теллур | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p4 |
| 53 | I | йод | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5 |
| 54 | Xe | ксенон | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 |
| № | Знак | Элемент | Электронная формула |
| VI период | |||
| 55 | Cs | цезий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s1 |
| 56 | Ba | барий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 |
| 57 | La | лантан | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 5d1 |
| 58 | Ce | церий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f2 |
| 59 | Pr | празеодим | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f3 |
| 60 | Nd | неодим | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f4 |
| 61 | Pm | прометий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f5 |
| 62 | Sm | самарий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f6 |
| 63 | Eu | европий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f7 |
| 64 | Gd | гадолиний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f7 5d1 |
| 65 | Tb | тербий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f9 |
| 66 | Dy | диспрозий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f10 |
| 67 | Ho | гольмий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f11 |
| 68 | Er | эрбий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f12 |
| 68 | Tm | тулий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f13 |
| 70 | Yb | иттербий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 |
| 71 | Lu | лютеций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d1 |
| 72 | Hf | гафний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d2 |
| 73 | Ta | тантал | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d3 |
| 74 | W | вольфрам | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d4 |
| 75 | Re | рений | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d5 |
| 76 | Os | осмий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d6 |
| 77 | Ir | иридий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d7 |
| 78 | Pt | платина | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s1 4f14 5d9 |
| 79 | Au | золото | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s1 4f14 5d10 |
| 80 | Hg | ртуть | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 |
| 81 | Tl | таллий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p1 |
| 82 | Pb | свинец | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p2 |
| 83 | Bi | висмут | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p3 |
| 84 | Po | полоний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p4 |
| 85 | At | астат | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p5 |
| 86 | Rn | радон | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10 5p6 6s2 4f14 5d10 6p6 |
| № | Знак | Элемент | Электронная формула |
| VII период | |||
| 87 | Fr | франций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s1 |
| 88 | Ra | радий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 |
| 89 | Ac | актиний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 6d1 |
| 90 | Th | торий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 6d2 5f0 |
| 91 | Pa | протактиний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f2 6d1 |
| 92 | U | уран | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f3 6d1 |
| 93 | Np | нептуний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f4 6d1 |
| 94 | Pu | плутоний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f5 6d1 |
| 95 | Am | америций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f7 |
| 96 | Cm | кюрий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f7 6d1 |
| 97 | Bk | берклий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f8 6d1 |
| 98 | Cf | калифорний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f10 |
| 99 | Es | эйнштейний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f11 |
| 100 | Fm | фермий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f12 |
| 101 | Md | менделеевий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f13 |
| 102 | No | нобелий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 |
| 103 | Lr | лоуренсий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d1 |
| 104 | Rf | резерфордий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d2 |
| 105 | Db | дубний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d3 |
| 106 | Sg | сиборгий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d4 |
| 107 | Bh | борий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d5 |
| 108 | Hs | хассий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d6 |
| 109 | Mt | мейтнерий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d7 |
| 110 | Ds | дармштадтий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d8 |
| 111 | Rg | рентгений | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d9 |
| 112 | Cn | коперниций | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 |
| 113 | Nh | нихоний | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p1 |
| 114 | Fl | флеровий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p2 |
| 115 | Mс | московий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p3 |
| 116 | Lv | ливерморий | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p4 |
| 117 | Ts | теннесcин | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p5 |
| 118 | Og | оганесон | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6 |
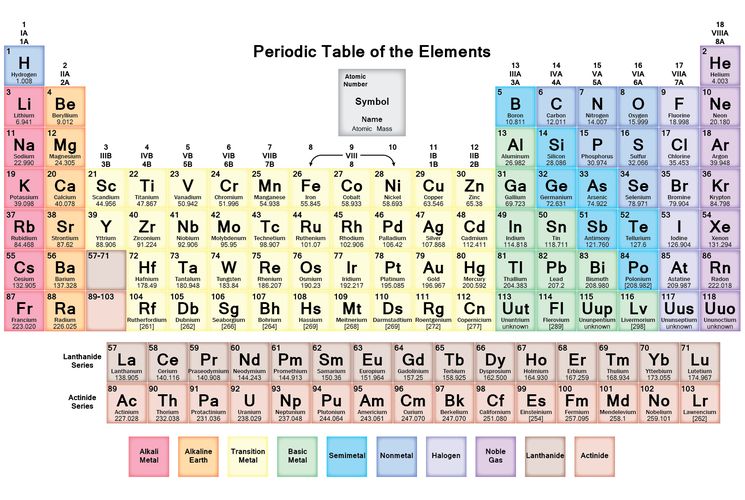
Электронные конфигурации элементов со 105 по 118
Электронные конфигурации элементов со 105 по 118 приведены согласно данных сайта WebElements
- 105 Db : [Rn].5f14.6d3.7s2 (догадка, основанная на электронной конфигурации тантала) ; 2.8.18.32.32.11.2
- 106 Sg : [Rn].5f14.6d4.7s2 (догадка, основанная на электронной конфигурации вольфрама) ; 2.8.18.32.32.12.2
- 107 Bh : [Rn].5f14.6d5.7s2 (догадка, основанная на электронной конфигурации рения) ; 2.8.18.32.32.13.2
- 108 Hs : [Rn].5f14.6d6.7s2 (догадка, основанная на электронной конфигурации осмия) ; 2.8.18.32.32.14.2
- 109 Mt : [Rn].5f14.6d7.7s2 (догадка, основанная на электронной конфигурации иридия) ; 2.8.18.32.32.15.2
- 110 Ds : [Rn].5f14.6d9.7s1 (догадка, основанная на электронной конфигурации платины) ; 2.8.18.32.32.17.1
- 111 Rg : [Rn].5f14.6d10.7s1 (догадка, основанная на электронной конфигурации золота) ; 2.8.18.32.32.18.1
- 112 Cn : [Rn].5f14.6d10.7s2 (догадка, основанная на электронной конфигурации ртути) ; 2.8.18.32.32.18.2
- 113 Uut : [Rn].5f14.6d10.7s2.7p1 (догадка, основанная на электронной конфигурации таллия) ; 2.8.18.32.32.18.3
- 114 Fl : [Rn].5f14.6d10.7s2.7p2 (догадка, основанная на электронной конфигурации свинца) ; 2.8.18.32.32.18.4
- 115 Uup : [Rn].5f14.6d10.7s2.7p3 (догадка, основанная на электронной конфигурации висмута) ; 2.8.18.32.32.18.5
- 116 Lv : [Rn].5f14.6d10.7s2.7p4 (догадка, основанная на электронной конфигурации полония) ; 2.8.18.32.32.18.6
- 117 Uus : [Rn].5f14.6d10.7s2.7p5 (догадка, основанная на электронной конфигурации астата) ; 2.8.18.32.32.18.7
- 118 Uuo : [Rn].5f14.6d10.7s2.7p6 (догадка, основанная на электронной конфигурации радона) ; 2.8.18.32.32.18.8
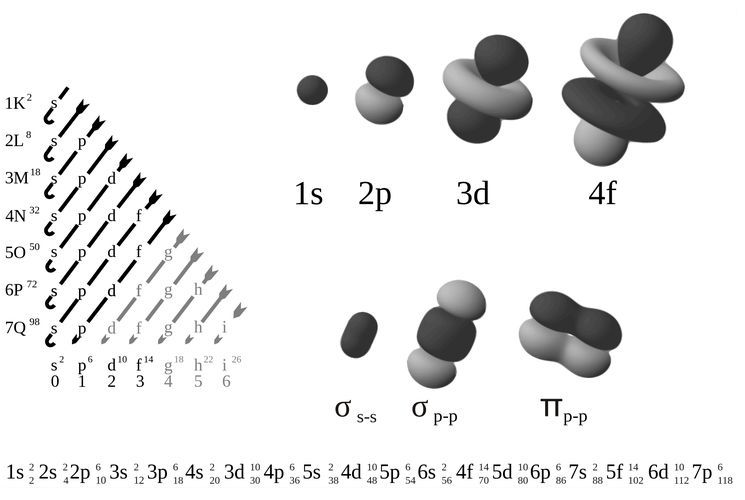
Эмпирическое правило Клечковского
Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречат реальной энергетической последовательности атомных орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место «провал» электрона с s-подуровня внешнего слоя на d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, а именно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d, а не 4f, и только затем происходит заселение четырнадцатью электронами орбиталей 4f, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и для орбиталей 7s, 6d и 5f.
Источники:
- Atomic, Molecular, & Optical Physics Handbook, Ed. Gordon W. F. Drake, American Institute of Physics, Woodbury, New York, USA, 1996.
- R.L. DeKock and H.B. Gray in Chemical Structure and bonding, Benjamin/Cummings, Menlo Park, California, USA, 1980.
- A.M. James and M.P. Lord in Macmillan’s Chemical and Physical Data, Macmillan, London, UK, 1992.
- J.E. Huheey, E.A. Keiter, and R.L. Keiter in Inorganic Chemistry : Principles of Structure and Reactivity, 4th edition, HarperCollins, New York, USA, 1993.
www.sciencedebate2008.com
| № элемента | Химический знак | Название элемента | Электронная формула |
| 1 | H | водород | 1s1 |
| 2 | He | гелий | 1s2 |
| II период | |||
| 3 | Li | литий | 1s22s1 |
| 4 | Be | бериллий | 1s22s2 |
| 5 | B | бор | 1s22s22p1 |
| 6 | C | углерод | 1s22s22p2 |
| 7 | N | азот | 1s22s22p3 |
| 8 | O | кислород | 1s22s22p4 |
| 9 | F | фтор | 1s22s22p5 |
| 10 | Ne | неон | 1s22s22p6 |
| III период | |||
| 11 | Na | натрий | 1s22s22p63s1 |
| 12 | Mg | магний | 1s22s22p63s2 |
| 13 | Al | алюминий | 1s22s22p63s23p1 |
| 14 | Si | кремний | 1s22s22p63s23p2 |
| 15 | P | фосфор | 1s22s22p63s23p3 |
| 16 | S | сера | 1s22s22p63s23p4 |
| 17 | Cl | хлор | 1s22s22p63s23p5 |
| 18 | Ar | аргон | 1s22s22p63s23p6 |
| IV период | |||
| 19 | K | калий | 1s22s22p63s23p64s1 |
| 20 | Ca | кальций | 1s22s22p63s23p64s2 |
| 21 | Sc | скандий | 1s22s22p63s23p64s23d1 |
| 22 | Ti | титан | 1s22s22p63s23p64s23d2 |
| 23 | V | ванадий | 1s22s22p63s23p64s23d3 |
| 24 | Cr | хром | 1s22s22p63s23p64s13d5 |
| 25 | Mn | марганец | 1s22s22p63s23p64s23d5 |
| 26 | Fe | железо | 1s22s22p63s23p64s23d6 |
| 27 | Co | кобальт | 1s22s22p63s23p64s23d7 |
| 28 | Ni | никель | 1s22s22p63s23p64s23d8 |
| 29 | Cu | медь | 1s22s22p63s23p64s13d10 |
| 30 | Zn | цинк | 1s22s22p63s23p64s23d10 |
| 31 | Ga | галлий | 1s22s22p63s23p64s23d104p1 |
| 32 | Ge | германий | 1s22s22p63s23p64s23d104p2 |
| 33 | As | мышьяк | 1s22s22p63s23p64s23d104p3 |
| 34 | Se | селен | 1s22s22p63s23p64s23d104p4 |
| 35 | Br | бром | 1s22s22p63s23p64s23d104p5 |
| 36 | Kr | криптон | 1s22s22p63s23p64s23d104p6 |
| V период | |||
| 37 | Rb | рубидий | 1s 22s 22p 63s 23p64s 23d104p65s1 |
| 38 | Sr | стронций | 1s 22s 22p 63s 23p64s 23d104p65s2 |
| 39 | Y | иттрий | 1s 22s 22p 63s 23p64s 23d104p65s24d1 |
| 40 | Zr | цирконий | 1s 22s 22p 63s 23p64s 23d104p65s24d2 |
| 41 | Nb | ниобий | 1s 22s 22p 63s 23p64s 23d104p65s14d4 |
| 42 | Mo | молибден | 1s 22s 22p 63s 23p64s 23d104p65s14d5 |
| 43 | Tc | технеций | 1s 22s 22p 63s 23p64s 23d104p65s24d5 |
| 44 | Ru | рутений | 1s 22s 22p 63s 23p64s 23d104p65s14d7 |
| 45 | Rh | родий | 1s 22s 22p 63s 23p64s 23d104p65s14d8 |
| 46 | Pd | палладий | 1s 22s 22p 63s 23p64s 23d104p65s04d10 |
| 47 | Ag | серебро | 1s 22s 22p 63s 23p64s 23d104p65s14d10 |
| 48 | Cd | кадмий | 1s 22s 22p 63s 23p64s 23d104p65s24d10 |
| 49 | In | индий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p1 |
| 50 | Sn | олово | 1s 22s 22p 63s 23p64s 23d104p65s24d105p2 |
| 51 | Sb | сурьма | 1s 22s 22p 63s 23p64s 23d104p65s224d105p3 |
| 52 | Te | теллур | 1s 22s 22p 63s 23p64s 23d104p65s24d105p4 |
| 53 | I | йод | 1s 22s 22p 63s 23p64s 23d104p65s24d105p5 |
| 54 | Xe | ксенон | 1s 22s 22p 63s 23p64s 23d104p65s24d105p6 |
| VI период | |||
| 55 | Cs | цезий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s1 |
| 56 | Ba | барий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s2 |
| 57 | La | лантан | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s25d1 |
| 58 | Ce | церий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f2 |
| 59 | Pr | празеодим | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f3 |
| 60 | Nd | неодим | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f4 |
| 61 | Pm | прометий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f5 |
| 62 | Sm | самарий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f6 |
| 63 | Eu | европий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f7 |
| 64 | Gd | гадолиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f75d1 |
| 65 | Tb | тербий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f9 |
| 66 | Dy | диспрозий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f10 |
| 67 | Ho | гольмий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f11 |
| 68 | Er | эрбий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f12 |
| 68 | Tm | тулий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f13 |
| 70 | Yb | иттербий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f14 |
| 71 | Lu | лютеций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d1 |
| 72 | Hf | гафний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d2 |
| 73 | Ta | тантал | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d3 |
| 74 | W | вольфрам | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d4 |
| 75 | Re | рений | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d5 |
| 76 | Os | осмий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d6 |
| 77 | Ir | иридий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d7 |
| 78 | Pt | платина | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s14f145d9 |
| 79 | Au | золото | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s14f145d10 |
| 80 | Hg | ртуть | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d10 |
| 81 | Tl | таллий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p1 |
| 82 | Pb | свинец | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p2 |
| 83 | Bi | висмут | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p3 |
| 84 | Po | полоний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p4 |
| 85 | At | астат | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p5 |
| 86 | Rn | радон | 1s 22s 22p 63s 23p64s 23d104p65s14d105p66s24f145d106p6 |
| VII период | |||
| 87 | Fr | франций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s1 |
| 88 | Ra | радий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s2 |
| 89 | Ac | актиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s26d1 |
| 90 | Th | торий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s26d25f0 |
| 91 | Pa | протактиний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f26d1 |
| 92 | U | уран | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f36d1 |
| 93 | Np | нептуний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f46d1 |
| 94 | Pu | плутоний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f56d1 |
| 95 | Am | америций | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f7 |
| 96 | Cm | кюрий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f76d1 |
| 97 | Bk | берклий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f86d1 |
| 98 | Cf | калифорний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f10 |
| 99 | Es | эйнштейний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f11 |
| 100 | Fm | фермий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f12 |
| 101 | Md | менделеевий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f13 |
| 102 | No | нобелий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f14 |
| 103 | Lr | лоуренсий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d1 |
| 104 | Rf | резерфордий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d2 |
| 105 | Db | дубний | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d3 |
| 106 | Sg | сиборгий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d4 |
| 107 | Bh | борий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d5 |
| 108 | Hs | хассий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d6 |
| 109 | Mt | мейтнерий | 1s 22s 22p 63s 23p64s 23d104p65s24d105p66s24f145d106p67s25f146d7 |
| s-элементы | p-элементы | d-элементы | f-элементы |
infotables.ru
Как составить электронную формулу химического элемента в неорганической химии
Выясним, как составить электронную формулу химического элемента. Этот вопрос является важным и актуальным, так как дает представление не только о строении, но и о предполагаемых физических и химических свойствах рассматриваемого атома.
Правила составления
Для того чтобы составить графическую и электронную формулу химического элемента, необходимо иметь представление о теории строения атома. Начнем с того, что есть два основных компонента атома: ядро и отрицательные электроны. Ядро включает в себя нейтроны, которые не имеют заряда, а также протоны, обладающие положительным зарядом.Рассуждая, как составить и определить электронную формулу химического элемента, отметим, что для нахождения числа протонов в ядре, потребуется периодическая система Менделеева.Номер элемента по порядку соответствует количеству протонов, находящихся в его ядре. Номер периода, в котором располагается атом, характеризует число энергетических слоев, располагаются на которых электроны.Для определения количества нейтронов, лишенных электрического заряда, необходимо из величины относительной массы атома элемента, отнять его порядковый номер (количество протонов).
Инструкция
Для того чтобы понять, как составить электронную формулу химического элемента, рассмотрим правило заполнения отрицательными частицами подуровней, сформулированное Клечковским.В зависимости от того, каким запасом свободной энергии обладают свободные орбитали, составляется ряд, характеризующий последовательность заполнения уровней электронами.Каждая орбиталь содержит всего два электрона, которые располагаются антипараллельными спинами.Для того чтобы выразить структуру электронных оболочек, применяют графические формулы. Как выглядят электронные формулы атомов химических элементов? Как составлять графические варианты? Эти вопросы включены в школьный курс химии, поэтому остановимся на них подробнее.Существует определенная матрица (основа), которую используют при составлении графических формул. Для s-орбитали характерна только одна квантовая ячейка, в которой противоположно друг другу располагается два электрона. Их в графическом виде обозначаются стрелками. Для р-орбитали изображают три ячейки, в каждой также находится по два электрона, на d орбитали располагается десять электронов, а f заполняется четырнадцатью электронами.
Примеры составления электронных формул
Продолжим разговор о том, как составить электронную формулу химического элемента. Например, нужно составить графическую и электронную формулу для элемента марганца. Сначала определим положение данного элемента в периодической системе. Он имеет 25 порядковый номер, следовательно, в атоме располагается 25 электронов. Марганец - это элемент четвертого периода, следовательно, у него четыре энергетических уровня.Как составить электронную формулу химического элемента? Записываем знак элемента, а также его порядковый номер. Пользуясь правилом Клечковского, распределяем по энергетическим уровням и подуровням электроны. Последовательно располагаем их на первом, втором, а также третьем уровне, вписывая в каждую ячейку по два электрона.Далее суммируем их, получая 20 штук. Три уровня в полном объеме заполнены электронами, а на четвертом остается только пять электронов. Учитывая, что для каждого вида орбитали характерен свой запас энергии, оставшиеся электроны распределяем на 4s и 3d подуровень. В итоге готовая электронно-графическая формула для атома марганца имеет следующий вид:1s2 / 2s2, 2p6 / 3s2, 3p6 / 4s2, 3d3
Практическое значение
С помощью электронно-графических формул можно наглядно увидеть число свободных (неспаренных) электронов, определяющих валентность данного химического элемента.Предлагаем обобщенный алгоритм действий, с помощью которого можно составить электронно-графические формулы любых атомов, располагающихся в таблице Менделеева.В первую очередь необходимо определить количество электронов, используя периодическую систему. Цифра периода указывает на численность энергетических уровней.Принадлежность к определенной группе связана с количеством электронов, находящихся на наружном энергетическом уровне. Подразделяют уровни на подуровни, заполняют их с учетом правила Клечковского.
Заключение
Для того чтобы определить валентные возможности любого химического элемента, расположенного в таблице Менделеева, необходимо составить электронно-графическую формулу его атома. Алгоритм, приведенный выше, позволит справиться с поставленной задачей, определить возможные химические и физические свойства атома.Источник
www.obovsyom.ru
Как составить электронную формулу химического элемента в неорганической химии
Выясним, как составить электронную формулу химического элемента. Этот вопрос является важным и актуальным, так как дает представление не только о строении, но и о предполагаемых физических и химических свойствах рассматриваемого атома.Для того чтобы составить графическую и электронную формулу химического элемента, необходимо иметь представление о теории строения атома. Начнем с того, что есть два основных компонента атома: ядро и отрицательные электроны. Ядро включает в себя нейтроны, которые не имеют заряда, а также протоны, обладающие положительным зарядом.Рассуждая, как составить и определить электронную формулу химического элемента, отметим, что для нахождения числа протонов в ядре, потребуется периодическая система Менделеева.Номер элемента по порядку соответствует количеству протонов, находящихся в его ядре. Номер периода, в котором располагается атом, характеризует число энергетических слоев, располагаются на которых электроны.Для определения количества нейтронов, лишенных электрического заряда, необходимо из величины относительной массы атома элемента, отнять его порядковый номер (количество протонов).1Для того чтобы понять, как составить электронную формулу химического элемента, рассмотрим правило заполнения отрицательными частицами подуровней, сформулированное Клечковским.В зависимости от того, каким запасом свободной энергии обладают свободные орбитали, составляется ряд, характеризующий последовательность заполнения уровней электронами.Каждая орбиталь содержит всего два электрона, которые располагаются антипараллельными спинами.Для того чтобы выразить структуру электронных оболочек, применяют графические формулы. Как выглядят электронные формулы атомов химических элементов? Как составлять графические варианты? Эти вопросы включены в школьный курс химии, поэтому остановимся на них подробнее.Существует определенная матрица (основа), которую используют при составлении графических формул. Для s-орбитали характерна только одна квантовая ячейка, в которой противоположно друг другу располагается два электрона. Их в графическом виде обозначаются стрелками. Для р-орбитали изображают три ячейки, в каждой также находится по два электрона, на d орбитали располагается десять электронов, а f заполняется четырнадцатью электронами.2Продолжим разговор о том, как составить электронную формулу химического элемента. Например, нужно составить графическую и электронную формулу для элемента марганца. Сначала определим положение данного элемента в периодической системе. Он имеет 25 порядковый номер, следовательно, в атоме располагается 25 электронов. Марганец - это элемент четвертого периода, следовательно, у него четыре энергетических уровня.Как составить электронную формулу химического элемента? Записываем знак элемента, а также его порядковый номер. Пользуясь правилом Клечковского, распределяем по энергетическим уровням и подуровням электроны. Последовательно располагаем их на первом, втором, а также третьем уровне, вписывая в каждую ячейку по два электрона.Далее суммируем их, получая 20 штук. Три уровня в полном объеме заполнены электронами, а на четвертом остается только пять электронов. Учитывая, что для каждого вида орбитали характерен свой запас энергии, оставшиеся электроны распределяем на 4s и 3d подуровень. В итоге готовая электронно-графическая формула для атома марганца имеет следующий вид:1s2 / 2s2, 2p6 / 3s2, 3p6 / 4s2, 3d33С помощью электронно-графических формул можно наглядно увидеть число свободных (неспаренных) электронов, определяющих валентность данного химического элемента.Предлагаем обобщенный алгоритм действий, с помощью которого можно составить электронно-графические формулы любых атомов, располагающихся в таблице Менделеева.В первую очередь необходимо определить количество электронов, используя периодическую систему. Цифра периода указывает на численность энергетических уровней.Принадлежность к определенной группе связана с количеством электронов, находящихся на наружном энергетическом уровне. Подразделяют уровни на подуровни, заполняют их с учетом правила Клечковского.4Для того чтобы определить валентные возможности любого химического элемента, расположенного в таблице Менделеева, необходимо составить электронно-графическую формулу его атома. Алгоритм, приведенный выше, позволит справиться с поставленной задачей, определить возможные химические и физические свойства атома.Вы ещё не оставляли комментарий к данной публикации. Поделитесь Вашим мнением.
mblshkoblud.ru